
某兴趣小组对硫酸厂排放的废水中硫酸含量进行检测:
(1)配制溶液:配制溶质质量分数为4%的NaOH溶液20g,需要NaOH固体 g,水 ml(水的密度为1g/cm3);
(2)检测分析:取废水样品98g,恰好与配制的20gNaOH溶液完全反应,试计算废水中硫酸的质量分数。(假设废水中其它成分均不和NaOH反应,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O).
【解析】
试题分析:(1)根据溶质质量等于溶液质量和溶质质量分数的乘积进行分析;
(2)根据 ×100%,求出废水中硫酸的质量分数。
×100%,求出废水中硫酸的质量分数。
解:(1)溶质质量=溶液质量×溶质质量分数=20g×4%=0.8g,所以溶剂质量为:20g-0.8g=19.2g,故需水的体积为 =19.2ml,故需水19.2ml。
=19.2ml,故需水19.2ml。
(2)氢氧化钠的质量=20g×4%=0.8g
设硫酸的质量为x
H2SO4+2NaOH=Na2SO4+2H2O
98 80
x 0.8g
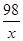 =
=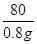
X=0.98g
废水中硫酸的质量分数=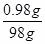 ×100%=1%
×100%=1%
答:废水中硫酸的质量分数为1%。
考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算


科目:初中化学 来源: 题型:
右图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是( )
A. 集气瓶内加入少量水可防止瓶底炸裂
B. 该实验所用红磷的量不足可能造成气体减少的体积小于五分 之一
C. 实验时,点燃的红磷要立即伸入集气瓶中,并塞紧橡胶塞
D. 红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹
查看答案和解析>>
科目:初中化学 来源: 题型:
20℃时,硝酸钾的溶解度为31.6 g,在该温度下,将10 g 硝酸钾加入10 g水所形成溶液中溶质的质量分数约为( )
| A.20% | B.24% | C.31.6% | D.50% |
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学在四个烧杯中分别做有关溶液实验,依据表格回答问题。
| 烧杯序号 | 温度/℃ | 水的质量/g | 硝酸钾质量/g | 溶液质量/ |
| ① | 20 | 50 | 10 | 60 |
| ② | 20 | 100 | 30 | a |
| ③ | 20 | 100 | 36 | 131.6 |
| ④ | 30 | 100 | 45 | 145 |
(1)硝酸钾溶液中的溶剂是__________。
(2)20℃时硝酸钾的溶解度是 g,a为 。
(3)将烧杯①所得溶液稀释成溶质的质量分数为10%的溶液,需要加水 g。
(4)若使烧杯③溶液中溶质的质量分数增大,可继续__________(填字母序号)。
A.加入少量硝酸钾
B.再加10g水
C.恒温蒸发部分溶剂
D.升温到30℃
E. 加入100 g 30℃时硝酸钾的饱和溶液,再恢复至20℃
查看答案和解析>>
科目:初中化学 来源: 题型:
下列是小明同学配制100 g 10% NaCl溶液的实验操作示意图。
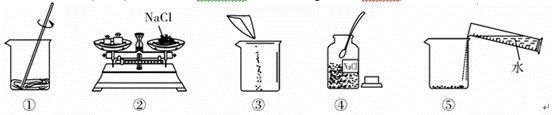
(1)该实验正确的操作顺序是____________(填序号)。
(2)认真观察指出图中错误的操作步骤________(填序号)。
(3)配制该溶液需要NaCl固体________g,需要水________mL(ρ水=1 g/mL)。
(4)小明同学将称量完毕的食盐转移到烧杯里时,不慎将少量食盐洒落在桌面上,这样会使所配制的溶液中溶质质量分数________10%(填“>”“=”或“<”)。
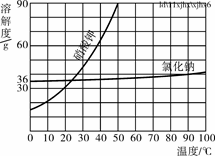
(5)部分物质溶解度曲线如右图所示,在20 ℃时,将40 g NaCl固体加入到100 g水中,搅拌使其充分溶解,你认为所得NaCl溶液的质量是________g,溶质质量分数是________%(精确到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com