
分析 (1)所有的化学变化都遵循质量守恒定律;
【实验探究】氮化镁与水反应会生成氨气;
【反思与交流】①根据镁的性质可以判断能否利用镁燃烧测定空气中氧气的含量;
②根据氧气和氮气的化学性质进行分析.
解答 解:(1)在点燃的条件下,镁与氧气反应生成氧化镁,相关符号表达式为:2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO;
该反应遵守质量守恒定律;镁条在空气中燃烧有氧气参与,使燃烧产物的质量大于反应物镁条的质量;
【实验探究】氮化镁与水反应会生成氨气,氨气能使湿润的红色石蕊试纸变蓝色;反应的化学方程式为:3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
【反思与交流】①因为镁燃烧时,能够同时和空气中的氧气、氮气发生化学反应,消耗的气体大于空气体积的1/5,因此不能用镁测定空气中氧气的含量.
②氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应,所以镁条在空气中燃烧生成的氧化镁却远多于氮化镁.
故答案为:(1)2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO;遵守;
【实验探究】试纸变蓝色;3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
【反思与交流】①大于;②氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
点评 在应用质量守恒定律时,一定要分清反应物和生成物,不能忽略气体物质的质量.验证质量守恒定律,条件的控制是关键,一般用密闭容器进行实验,称量前后容器的质量变化.


科目:初中化学 来源: 题型:选择题
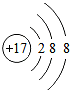
| A. | 该元素的原子在化学反应中容易失去电子 | |
| B. | 该粒子是阳离子 | |
| C. | 该元素原子核内质子数为17 | |
| D. | 该元素原子的最外层上有8个电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素是三种元素组成的化合物 | |
| B. | 一个青蒿素分子中含有42个原子 | |
| C. | 表示一个青蒿素分子 | |
| D. | 青高素是由15个碳原子、22个氢原子和5个氧原子构成的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com