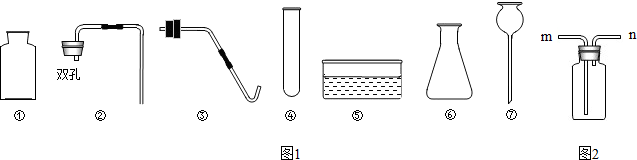
解答:解:(1)氢气在空气中燃烧生成水,反应的化学方程式为:2H
2+O
2 2H
2O;
氢气在氧气中燃烧,产生淡蓝色火焰,集气瓶内壁有水雾出现,可得出水由氢氧两种元素组成;
②Ⅰ、A、氧化钙溶于水,生成氢氧化钙,溶液成为氢氧化钙溶液,故错误;
B、胆矾是硫酸铜的晶体,溶于水后溶质是硫酸铜,溶液成为硫酸铜溶液,故错误;
C、氢氧化钠溶于水,溶液成为氢氧化钠溶液,故错误;
D、氯化钠俗名食盐,溶液成为食盐溶液,正确;
Ⅱ、配制不高于20%的溶液质量≥
=2.5g
则加入蒸馏水的质量≥2.5g-0.5g=2g
由于水的密度是1g/ml所以需水的体积至少为2mL.
Ⅲ、根据溶解度曲线,t
4℃时,甲、乙两物质的溶解度曲线交于一点,二者的溶解度相等;
甲溶液从a点降温至b点,甲溶液从不饱和溶液转化为饱和溶液,但是溶质、溶剂、溶液质量都没变;由于温度减低,溶解度减小,
饱和溶液的质量分数可以用该公式计算:
×100%,所以饱和溶液的质量分数取决于溶解度的大小,t
1℃时甲、乙两种物质溶解度乙>甲所以饱和溶液溶质质量分数也是乙>甲,升温后甲、乙两种物质的溶质质量分数不变所以温度升高到t
2℃后饱和溶液溶质质量分数还是乙>甲;由于丙物质的饱和溶液升温后会析出晶体,所以升温后丙的溶质质量分数取决于丙在t
4℃的溶解度,因为溶解度的大小为:乙=甲>丙,所以温度升高到t
4℃后(升温过程中溶剂量不变),三种溶液中溶质的质量分数由大到小的顺序是乙>甲>丙.
③制取碳酸饮料过程中二氧化碳与水反应生成碳酸,方程式为:CO
2+H
2O═H
2CO
3.
灭火时将水喷成细雾状的主要原因增大与可燃物接触面积来隔绝空气.
故答案为:①2H
2+O
2 2H
2O;产生淡蓝色火焰,集气瓶内壁有水雾出现;氢氧两种;
②Ⅰ.D;Ⅱ.2;Ⅲ.t
4;AB;乙>甲>丙;
③CO
2+H
2O═H
2CO
3;B.



 习题精选系列答案
习题精选系列答案