
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 40 | 5 |
| 反应后质量/g | 待测 | 24 | 8 | 23 |
| A. | 该反应的类型是置换反应 | B. | Y、Q的相对分子质量比为11:9 | ||
| C. | 反应后X的质量为10g | D. | 参加反应的X、Z的质量比为1:4 |
分析 该题为一道图表和数据相结合的试题,首先根据质量守恒定律求出反应后X的质量(即待测处的数值)然后根据X、Y、Z、Q反应前后的质量变化确定出反应物和生成物,进而可判断该反应的类型,再根据X、Y、Z、Q反应前后质量的变化可求出X、Z的质量比,Y、Q的质量比.
解答 解:A、根据各物质反应前后质量的变化可知:Y、Q为生成物,X、Z为反应物.故反应为;X+Z→Y+Q 该反应不一定为置换反应,也可能是复分解反应.故不正确.
B、生成的Y、Q的质量分别为:24-2=22克和23-5=18克故其质量比为22:18=11:9,Y、Q的质量比为11:9,它们的相对分子质量比不一定为11:9.故不正确.
C、根据质量守恒定律,8+2+40+5=24+8+23+待测,则待测=0,故错误.
D、参加反应的X的质量为8-0=8克,Z的质量为:40-8=32克,故参加反应的X、Z的质量比为1:4,故正确
故选D.
点评 该题要求学生能从图表中找出有效的数据进行处理解答,考查了学生的观察和分析能力.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:实验探究题
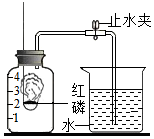 某同学设计了测定空气中氧气含量的实验,实验装置如右图.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并作好标记.②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.③充分反应后,待集气瓶冷却至室温,打开止水夹.请回答下列问题:
某同学设计了测定空气中氧气含量的实验,实验装置如右图.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并作好标记.②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.③充分反应后,待集气瓶冷却至室温,打开止水夹.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 鸡蛋 | B. | 馒头 | C. | 西红柿 | D. | 牛奶 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
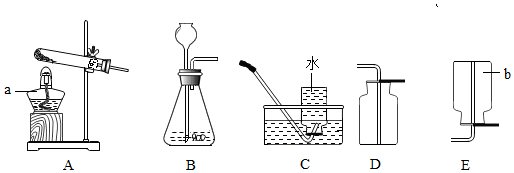
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①④⑦是混合物 | B. | ③⑥是化合物 | C. | ②④⑥是氧化物 | D. | ②⑤是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸的质量/g | 50 | 50 | 50 | 50 |
| 剩余固体的质量/g | 16.75 | 13.5 | m | 12.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com