某地1000Kg氮肥的市场价格如下:CO(NH2)2(尿素)1080元,NH4NO3810元,NH4HCO3(碳酸氢铵)330元.
(1)计算CO(NH2)2(尿素)的相对分子质量为:______.
(2)NH4HCO3(碳酸氢铵)中氮元素的质量分数:______.
(3)某农民承包农田的作物需要氮肥,要用1万元采购化肥,你建议他购买上述的哪一种?通过计算说明.
【答案】
分析:(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;(2)根据化合物中各元素质量分数=

×100%,进行解答;
(3)首先根据各种化肥的化学式计算N元素的质量分数,然后用N元素的质量分数乘以1万元钱分别购买的各种化肥的质量,得出氮元素的质量,进行比较,
如解法一:我们也可利用逆向思维的方法,让四种化肥提供一样多的N元素,求出四种化肥的质量比,然后根据单价,计算用钱最少的就是含N元素最多的;
(解法二):让四种化肥提供一样多的N元素,可从分子的角度考虑,提供相同个数的N原子.
解答:解:(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得CO(NH
2)
2(尿素)的相对分子质量为
12+16+(14+2)×2=60;故答案为:60;
(2)根据化合物中各元素质量分数=

×100%,可得
NH
4HCO
3(碳酸氢铵)中氮元素的质量分数为:
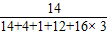
×100%=17.7%;
故答案为:17.7%;
(3)
(解法一)
CO(NH
2)
2中氮元素的质量分数=
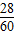
×100%=46.7%
10000元钱购买的该化肥中N元素的质量为:

×46.7%=4.32 吨----→①
NH
4NO
3中氮元素的质量分数=

×100%=35.0%
10000元钱购买的该化肥中N元素的质量为:

×35.0%=4.32 吨---→②
NH
4HCO
3中氮元素的质量分数=

×100%=17.7%
10000元钱购买的该化肥中N元素的质量为:
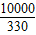
×17.7%=5.37 吨---→③
比较①②③,其中③最大,所以答案为:NH
4HCO
3;
(解法二)
提供一样多的N元素(从分子的角度考虑,都提供2个N原子),三种化肥的质量比为:
CO(NH
2)
2------NH
4NO
3------2NH
4HCO
3 60:80:158
30:40:79
该质量比的化肥用钱数之比:(30×1080):(40×810):(79×330)
32400:32400:26070
通过比较,提供一样多的N元素,购买NH
4HCO
3;花钱最少,那么花一样多的钱,购买NH
4HCO
3;所含N元素最多.
点评:该题主要考查根据化学式计算某元素的含量.善于从化学的微粒观考虑问题,能发散解题的思路,简化解题的过程.

 ×100%,进行解答;
×100%,进行解答; ×100%,可得
×100%,可得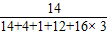 ×100%=17.7%;
×100%=17.7%;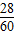 ×100%=46.7%
×100%=46.7% ×46.7%=4.32 吨----→①
×46.7%=4.32 吨----→① ×100%=35.0%
×100%=35.0% ×35.0%=4.32 吨---→②
×35.0%=4.32 吨---→② ×100%=17.7%
×100%=17.7%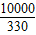 ×17.7%=5.37 吨---→③
×17.7%=5.37 吨---→③
