
分析 根据酸的性质与铁锈的成分进行分析,铁锈和硫酸反应能生成硫酸铁和水;根据钢铁的原理进行分析,防止机械进一步锈蚀可以在机械表面涂油漆.
解答 解:生锈的铁螺丝放入硫酸中,表面的铁锈(主要成分三氧化二铁)与硫酸反应生成硫酸铁与水,反应的化学方程式为:3H2SO4+Fe2O3═Fe2(SO4)3+3H2O.
金属在水和氧气同时接触容易生锈,所以隔绝氧气和水可以防止金属生锈.防止铁生锈有多种方法,如保持铁制品干燥、铁制品表面刷油漆等.在铁床表面涂油、刷漆等可以达到防止铁床生锈的目的.
故答案为:3H2SO4+Fe2O3═Fe2(SO4)3+3H2O;(去锈后)刷漆等.
点评 本题难度不大,掌握金属生锈的原因及防止金属生锈的方法、酸的化学性质等是正确解题的关键.


科目:初中化学 来源: 题型:实验探究题
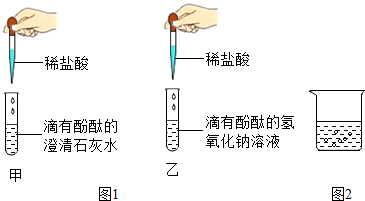
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
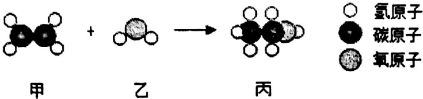
| A. | 甲的化学式为C2H4 | |
| B. | 保持乙化学性质的最小微粒是水分子 | |
| C. | 化学反应前后分子的种类都发生了改变 | |
| D. | 乙和丙都属于氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
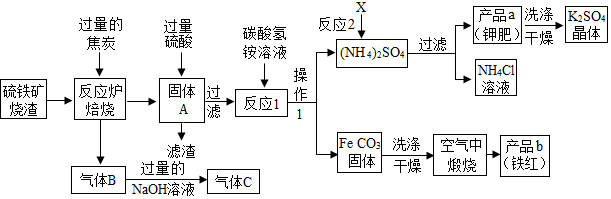
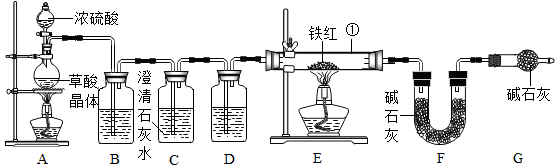
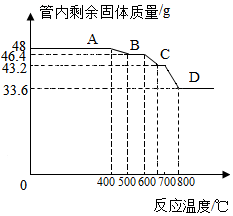
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com