
科目:初中化学 来源: 题型:选择题
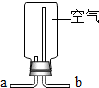 | 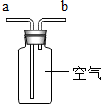 | 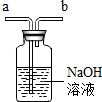 | 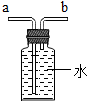 |
| 用排空气法收集CO2,则CO2从b管通入 | 用排空气法收集O2,则O2从a管通入 | 除去空气中的CO2,则空气从a管通入 | 用排水法收集O2,则O2从b管通入 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

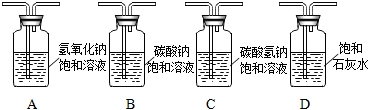
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
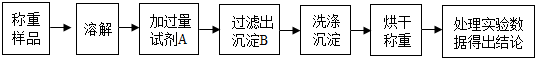
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱-①④ | B. | 纯净物-③④⑤ | C. | 混合物-②⑤ | D. | 盐-①⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 次数 | H2O2溶液质 量分数% | H2O2溶液用量 /毫升 | 催化剂(MnO2)用 量/克 | 反应温度 /℃ | 收集气体体积 /毫升 | 所需时间 /秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ④ | 30 | 5 | 0 | 55 | 2 | 10.5 |
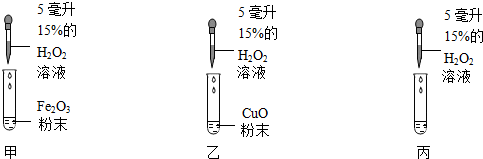
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com