
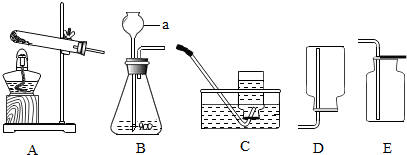
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
| ||
| ||


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| A、8g | B、6.4g |
| C、3.2g | D、6g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、11g | B、5.6g |
| C、2.8g | D、7.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:
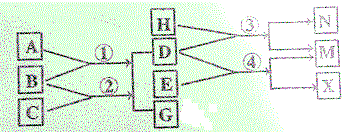 现有如图所示的转化关系.已知A、D、N、X为单质,其余为化合物,且B、X为红色固体.C、G、N为气体,M溶液为浅绿色.试推断后回答下列问题:
现有如图所示的转化关系.已知A、D、N、X为单质,其余为化合物,且B、X为红色固体.C、G、N为气体,M溶液为浅绿色.试推断后回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 提出假设 | 设计并完成实验 | 实验现象及结论 |
| 蜡烛的密度比水的密度 | 用小刀切下一小块蜡烛放在水中 | 蜡烛 |
| 蜡烛燃烧后生成了什么物质呢?假设蜡烛燃烧后生成了 | 在燃着的蜡烛上罩一个集气瓶,一会儿后迅速倒转过来,加入澄清石灰水,然后,在火焰的上罩一个 | 澄清石灰水变 |
| 蜡烛刚熄灭的白烟是石蜡小颗粒. | 用燃着的火柴去点燃蜡烛刚熄灭的白烟(火柴不要碰到蜡烛的烛心) | 蜡烛 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com