
【题目】大多数金属材料在空气中都会生锈.铜锈的主要成分是铜绿[Cu2(OH)2 CO3] .某同学利用如图所示的实验一进行实验,研究铜在空气中生锈的条件.一个月后该 同学发现B装置中的铜丝生锈了,而A、C装置中的铜丝无明显变化.
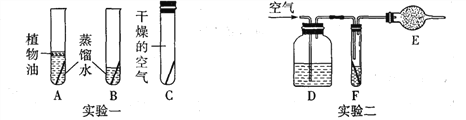
试回答下列问题:
(1)该同学得出结论说:“铜生锈的原因是铜与空气中的氧气和水相互作用.”该同学 得出的结论正确吗?_______,你认为影响铜生锈的因素还可能有____________.
(2)为了验证你的判断,现给你提供如图实验二所示的装置,从左到右每个仪器所盛 放的试剂依次为____________、__________和___________.(提示:E是干燥管)
(3)D、E中所加试剂的目的分别是________________________________.
【答案】 不正确 CO2 NaOH溶液[或Ca(OH)2溶液] 水 生石灰(或NaOH固体) D中Ca(OH)2溶液除去空气中的CO2,E中生石灰的作用是防止空气中的CO2和水蒸气进入F
【解析】(1)根据铜锈的化学式[Cu2(OH)2CO3],可以看出其中含有铜、氢、碳、氧四种元素,不会是只与氧气和水作用的结果,还应与含有碳元素的物质接触,而空气中的含碳物质主要是二氧化碳,所以铜生锈是铜与氧气、水、二氧化碳共同作用的结果;
(2)实验二是想验证铜生锈是否需要二氧化碳,所以可以通过除去空气中的二氧化碳,仅让铜与水和氧气接触,观看铜是否生锈来加以验证,要想除去空气中二氧化碳,可以通过氢氧化钠溶液[或Ca(OH)2溶液],所以广口瓶盛放的是氢氧化钠溶液[或Ca(OH)2溶液],为防止空气中的二氧化碳进入试管,可以在右边的干燥管内放入生石灰(或NaOH固体或碱石灰),试管中应放入水;
(3)D中Ca(OH)2溶液除去空气中的CO2,使实验结果更准确;E中生石灰的作用是防止空气中的CO2和水蒸气进入F。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】金属钛因为有神奇的性能越来越引起人们的关注。常温下钛不与非金属及强酸反应,加热时却可以和常见的非金属单质反应。钛是航空、军工、电力等工业领域的重要原材料。地壳中的钛矿石之一是金红石(主要成分是TiO2),目前大规模生产钛的方法是:
(1)使金红石与炭粉混合,在高温条件下反应,再通入氯气,制得TiCl4和一种可燃性气体。该反应的化学方程式是_____________________。
(2)在氩气的气流中,高温下用过量的镁和TiCl4反应可制得金属钛。写出该反应的化学方程式:___________________________________。
(3)从上述反应的混合物中分离出金属钛。写出简单的分离步骤和有关的化学方程式。_____________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
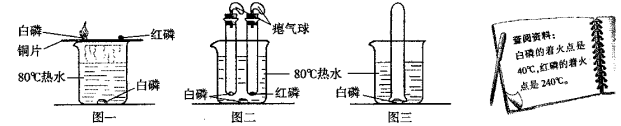
【知识回忆】可燃物燃烧的必备条件是 ;
【交流讨论】(1)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,因为钾遇水生成H2和一种碱(化学式为KOH),该反应是 (填“吸热”或“放热”)反应,其反应化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室常用甲酸(CHOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH![]() CO↑+H2O.下图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.
CO↑+H2O.下图是制备一氧化碳还原三氧化二铁并检验反应产物结束时的实验装置.
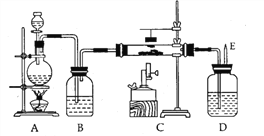
(1)先检查装置的气密性,实验开始应检验______________,以防爆炸.
(2)装置B中盛放_________,除去__________________;
(3)装置D中盛放____________,检验______________________;
(4)写出装置C中反应的化学方程式______________________;
(5)实验结束时应先停止___________处加热;
(6)在反应后磁铁悬在玻璃管上方,其中的作用是__________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧元素的结构示意图如图所示: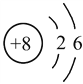
(1)该元素的原子核内质子数为__________;在化学反应中该原子容易_______电子(选填“得到”或“失去”);
(2)由该元素组成的一种气体单质能供给呼吸,写出实验室制取该气体的一个化学方程式:__________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)镁条在空气中燃烧,不仅生成氧化镁、氮化镁,还有少量镁与二氧化碳反应生成另一种单质和镁的氧化物。
(1)已知氮化镁中氮元素的化合价为-3价,请你写出生成氮化镁的化学反应式 。
(2)写出镁与二氧化碳反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】细铁丝在氧气中燃烧的现象是:剧烈燃烧,_________;放出大量热量;生成一种_____________。该反应的文字表达式是__________________ (__________反应)(填“分解”或“化合”)。做该实验时,集气瓶底应放_________,其目的是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白.
【提出问题】氧化铝能不能作过氧化氢分解的催化剂呢?
【作出猜想】氧化铝能作过氧化氢分解的催化剂.
【实验验证】
实验步骤 | 实验现象 | 实验结论 | |
实验一 | _______________ | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,然后将带火星的木条伸入试管中 | ________ | 氧化铝能加快过氧化氢的分解速率 |
【得出结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能作过氧化氢分解的催化剂.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
【实验目的】探究_______________________________________ 。
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行__________,洗涤,干燥,称量;④对比反应前后氧化铝的质量.
【交流讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究_____________________________________ 。
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铝对过氧化氢溶液分解的催化作用,其中观察效果最差的_________
|
|
|
|
第一组 | 第二组 | 第三组 | 第四组 |
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】唾液中含有较多的淀粉酶,新鲜猪肝中含有较多的过氧化氢酶,酶的催化作用具有高效性和专一性等特点。取五支试管,分别加入2.0 mL 30%的过氧化氢溶液,实验如下:

试回答下列问题:
(1)实验中产生的气泡的化学成分是_______,能促进过氧化氢分解的物质有___________________。
(2)1号试管和3号试管的实验结果比较,可说明酶具有_______性;2号试管和3号试管的实验结果比较,可以说明酶具有_______性。
(3)3号和4号、5号试管的实验结果比较,可以说明_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com