
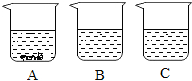
 A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入25g、15g、5g同种固体物质,充分溶解后,静置,现象如图所示,回答下列问题(填烧杯编号):
A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入25g、15g、5g同种固体物质,充分溶解后,静置,现象如图所示,回答下列问题(填烧杯编号):分析 (1)饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液;还能继续溶解这种溶质的溶液,叫做不饱和溶液.
(2)根据题意,等质量的水,在相同温度下,C烧杯中为该物质的不饱和溶液,B烧杯中溶解的溶质比C烧杯中多,可能是饱和溶液,也可能是不饱和溶液,据此进行分析解答.
解答 解:(1)由图可知,A中烧杯中残留有某固体物质,说明某固体物质不能继续溶解,说明该溶液一定为该温度下的饱和溶液;等质量的水,在相同温度下,B烧杯和C烧杯中分别溶解了15g、5g某固体物质,B烧杯中的溶液可能是饱和溶液,也可能是不饱和溶液;C烧杯中溶解的质量比B烧杯中的少,C烧杯中的溶液一定为不饱和溶液.
(2)等质量的水,在相同温度下,C烧杯中为该物质的不饱和溶液,B烧杯中溶解的溶质比C烧杯中多,可能是饱和溶液,也可能是不饱和溶液,若是饱和溶液,则AB烧杯中溶质的质量分数相同;若是不饱和溶液,则A烧杯中溶质的质量分数比B烧杯中溶质的质量分数大;即A≥B>C.
故答案为:(1)C;(2)A≥B>C.
点评 本题难度不大,掌握饱和溶液与不饱和溶液的特征、溶质的质量分数等是正确解答本题的关键.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:初中化学 来源: 题型:实验探究题
| 步骤 | 实验操作 | 实验现象 |
| 1 | 取少量固体于小烧杯中,加水充分溶解 | 固体全部溶解 |
| 2 | 取少量烧杯中的溶液于试管中,加入过量的 BaCl2溶液 | 产生白色沉淀 |
| 3 | 取少量2中的溶液于另一试管中,再加入少量FeCl3溶液 | 产生红褐色絮状沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 白磷保存在水中 | B. | 生石灰保存在烧杯中 | ||
| C. | 浓盐酸密封保存在试剂瓶中 | D. | 硝酸银溶液保存在棕色试剂瓶中 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  番茄、黄瓜 | B. |  米饭、土豆 | C. |  牛肉、鸡蛋 | D. |  色拉油、花生 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com