
分析 首先根据题意确定物质的化学名称,然后根据书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)氧气能供给呼吸,是用于医疗急救的气体,其化学式为:O2.
(2)人体中含量最多的物质是水,其化学式是H2O.(3)一氧化碳、二氧化硫等都有毒,是气体污染物,其化学式是CO(SO2).
(4)碳酸钠中的阴离子是碳酸根离子,其符号是CO32-.
(5)地壳中含量最多的金属元素是铝,最多的非金属元素是氧,两者形成的化合物是氧化铝,其化学式是Al2O3.故答案为:(1)O2;(2)H2O;(3)CO(SO2);(4)CO32-;(5)Al2O3.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在.


 名题金卷系列答案
名题金卷系列答案科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| Ⅰ、分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ、待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象. | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ、将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag. | |
| Ⅳ、分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某校研究性学习小组用如图装置进行镁条在空气中燃烧测定空气中氧气的体积分数,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧测定空气中氧气的体积分数,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%. 查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 用托盘天平称取11.87g粗盐 | B. | 用托盘天平称取11.7g粗盐 | ||
| C. | 用温度计测得温度为25.72℃ | D. | 用100mL量筒量取56.2mL水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
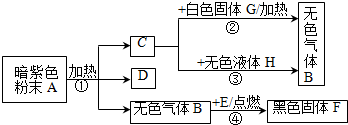
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
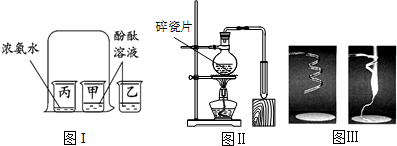
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
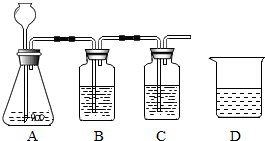 根据下列实验装置图回答问题:
根据下列实验装置图回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com