
【题目】超细碳酸钙可用于生产钙片、牙膏等产品。利用碳化法生产超细碳酸钙的主要流程示意如下:
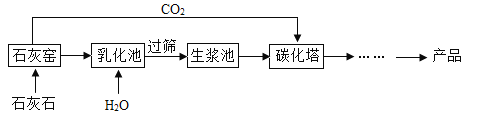
下列说法错误的是
A.这个流程中的反应都不需要消耗能量
B.乳化池中,生石灰与水发生反应,其化学方程式为CaO+H2O=Ca(OH)2
C.过筛的目的是拦截大于筛孔直径的颗粒,相当于基本实验操作中的过滤
D.碳化塔中的反应属于复分解反应
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图表示某些物质间转化关系。G为常见金属,E为赤铁矿的主要成分: C、 F都是由相同元素组成的无色气体,且C有毒: D、H都是无色气体单质:反应⑤是自然界中最重要的反应。请回答下列问题:
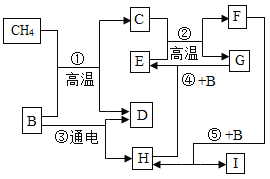
(1) B的化学式为_____________________;
(2)生活中为防止反应④的发生,可采取的措施是_____________________(写一 点即可)
(3)自然界中普遍存在反应⑤,该反应通常被称为_____________________;
(4)反应①的化学方程式为_____________________;反应②的化学方程式为_____________________;
(5)“绿色”特点之一是“零排放”。一定条件下, C和D两种气体可按照不同比例反应, 若只生成一种产物就能实现“零排放”,符合这一要求的产物是_____________________ (填字母) 。
A CH4O
B C2H6O
C C2H4O
D C2H4O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca10([PO4)6(OH)2]形式存在,其相对分子质量为1004,牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。如图是某品牌纯牛奶包装上的部分文字说明,请认真阅读后回答下列问题:

(1)一盒牛奶含钙至少_____g (精确到0.01)
(2)求羟基磷酸钙中钙元素的质量分数_____。(精确到0.1%)
(3)若人体每天至少需要0.6g钙,而这些钙有90%来自牛奶,则-一个人每天要喝多少盒牛奶?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质的溶解度曲线,下列说法不正确的是
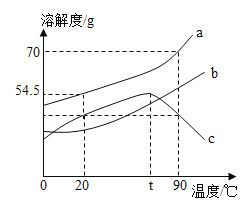
A.a属于易溶性物质
B.t℃时c物质的饱和溶液,可采用升高温度方法使其变为不饱和溶液
C.将20℃时三种物质的饱和溶液升温到90℃,所得溶液中溶质的质量分数的大小关系是:a>c>b
D.90℃时,将50ga加入到50g水中充分搅拌,可得到100g a的饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】农业生产上需要用200kg质量分数为16%的氯化钠溶液来进行选种。
(1)现有400kg20%的氯化钠溶液和400kg10%的氯化钠溶液,请通过计算回答该如何进行配制?____
(2)现有配制好的200kg16%的氯化钠溶液,取出其中的100kg溶液,要释成质量分数为8%的氯化钠溶液,需加水的质量是多少?______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸是一种重要的化工原料,初中化学中许多实验也都用到了硫酸。
(1)下列实验中一般不会用到硫酸的是______(填序号)。
A制铅酸蓄电池 B鉴别铁粉和氧化铜粉末
C实验室与石灰石反应制取二氧化碳 D除去铁钉上的锈迹
(2)5%的稀硫酸pH比10%的稀硫酸pH _____(填大或小)。
(3)某化学兴趣小组设计了下列两个实验:
实验一:证明硫酸与氢氧化钠反应是放热反应

甲同学设计如图所示的实验操作:根据实验,甲同学认为:NaOH与硫酸发生的中和反应是放热反应。乙同学认为:甲同学操作不正确且得出这个结论的依据不科学,操作不正确可能导致的后果是______,结论的依据不科学,应该用稀硫酸和氢氧化钠溶液反应,理由是:_______。乙同学改用稀硫酸溶液后,将氢氧化钠溶液滴到稀硫酸的过程中,若除了温度升高外还有________产生,则说明所用氢氧化钠溶液已变质。若要除去变质的NaOH溶液中的杂质,除杂所用试剂是________。
实验二:通过硫酸与氢氧化钠的反应测定未知浓度的氢氧化钠溶液中溶质质量分数
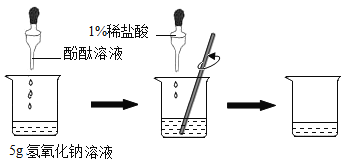
丙同学设计实验如下图所示:在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%稀硫酸,并不断搅拌,至溶液颜色恰好变为无色为止,共用去了稀硫酸9.8g,则所用氢氧化钠溶液中溶质的质量分数为多少?写出计算过程_______
(4)丁同学认为丙同学设计的实验中酚酞试液变成无色也可能是硫酸过量了,于是设计了以下实验验证,其中验证硫酸是否过量的方法中正确的是_____(填序号)。
A滴加氯化钡溶液看是否有白色沉淀产生
B测定溶液pH,看pH是否小于7
C加入蒸馏水,搅拌后看溶液是否变色
D加入金属铁片,看是否产生气泡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并作好标记.②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.③充分反应后,待集气瓶冷却至室温,打开止水夹。请回答下列问题:
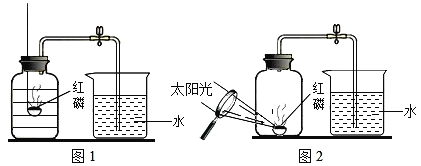
(1)该实验中红磷需稍过量,目的是___________。
(2)步骤②集气瓶中的现象是________,其反应的文字表达式为________;步骤③中打开止水夹后观察到的现象是_________,由此可得出空气中氧气的体积分数约为_____。
(3)小洁通过该实验测得的空气中氧气的体积分数与正常值相比偏小,其原因可能是_____
A 燃烧匙内可燃物量不足
B 装置气密性不好
C 未及时塞进橡胶塞
D 燃烧匙内可燃物有剩余
(4)该实验可推论出氮气_______(填“易”或“难”)溶于水和其化学性质_________(填“活泼”或“不活泼”)的结论.
(5)若将红磷换成炭粉,该实验能否获得成功?为什么?_____成功,原因是______。
(6)小华同学对实验进行反思后,提出了改进方法(如图2所示),你认为改进后的优点是:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究Fe、Cu、Ag的金属活动性强弱,某兴趣小组做了如下实验:
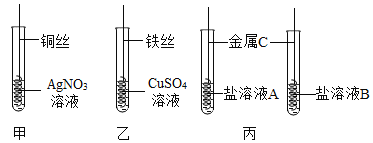
(1)实验前需将金属丝打磨,目的是_____。
(2)甲实验中发生反应的化学方程式为_____;乙实验中观察到的现象为_____。
(3)通过甲、乙实验探究,可得出三种金属活动性由强到弱的顺序为_____。
(4)若采用丙实验方案也可得出相同结论,则金属C是_____,A溶液与B溶液分别是_____和_____。
(5)如果只用两种金属丝和一种溶液,来探究三种金属的活动性强弱,则所需要的金属和溶液分别是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列微粒结构示意图及元素周期表中某元素的部分信息填空:
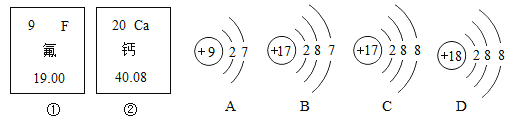
(1)含氟牙膏、补钙剂中的“氟”“钙”指的是______(选填“分子”“原子”或“元素”)。
(2)氟元素的原子核内质子数为_____,钙元素的相对原子质量是_______。
(3)A~D所示的粒子中化学性质相似的是_______,元素种类相同的是_______,其中属于离子的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com