
分析 (1)根据化学式改写成相应的氧化物的形式,按照活泼金属氧化物•较活泼金属氧化物•SiO2•H2O的顺序来书写,并要遵守原子守恒来分析解答.
(2)化学反应多数遵循强酸制备弱酸的原则.
解答 解:(1)①钾的氧化物为K2O,铝的氧化物为Al2O3,硅的氧化物为SiO2,则根据活泼金属氧化物•较活泼金属氧化物•SiO2•H2O的顺序可知,KAlSi3O8可改写为
K2O•Al2O3•6SiO2;故填:K2O•Al2O3•6SiO2;
②铝的氧化物为Al2O3,硅的氧化物为SiO2,氢的氧化物为H2O,则根据活泼金属氧化物•较活泼金属氧化物•SiO2•H2O的顺序可知,[Al2Si2O5(OH)4]可改成Al2O3•2SiO2•2H2O,故答案为:Al2O3•2SiO2•2H2O;
(2)碳酸可生成原硅酸,说明碳酸的酸性比原硅酸的强,故此反应发生的原因是碳酸酸性比硅酸强,由强酸可制得弱酸,故答案为:碳酸酸性比硅酸强,由强酸可制得弱酸.
点评 本题考查含硅矿物及材料的应用,注重将复杂化合物写出氧化物的形式的考查,注意要知道非金属元素氧化物的化学式的书写和先后顺序,还有遵循原子守恒定律,难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:解答题
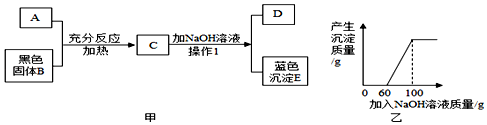
| 实验步骤 | 实验现象 | 结论 |
| 取少量无色滤液,向其中加入酚酞试液. | 溶液变红. | 你的猜想成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子、分子和离子都是构成物质的微粒 | |
| B. | 分子和原子都是不断运动的 | |
| C. | 原子都是由原子核和核外电子构成的 | |
| D. | 任何原子核都是由质子和中子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\frac{8(b+a)}{b-a}$ | B. | $\frac{16(b+a)}{b-a}$ | C. | $\frac{8(a-b)}{a+b}$ | D. | $\frac{a+b}{4}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭燃烧放热 | B. | 生石灰与水混合生成熟石灰放热 | ||
| C. | 白炽灯泡通电发热 | D. | 苹果腐烂发热 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
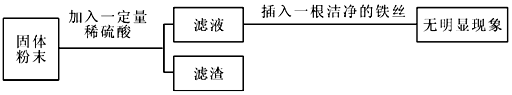
| A. | 向样品中加入稀硫酸后,一定有气体生成,且液体颜色不变 | |
| B. | 滤液中含有硫酸铜和硫酸亚铁 | |
| C. | 滤液中溶质只有硫酸亚铁 | |
| D. | 滤渣中一定有铜,不一定有铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
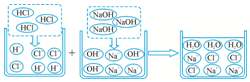
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com