
(3分)下图是浓盐酸试剂瓶标签的部分内容。请回答:

① 欲配制200g溶质质量分数为3.65%的稀盐酸,需要这种浓盐酸 g,体积为 mL。
②用①中所得稀盐酸与足量锌粒反应,请根据化学方程式计算最多可得氢气的质量
20 g, 16.9 mL。② 0.2克
解析:①配制200g溶质质量分数为3.65%的稀盐酸的溶质的质量:200×3.65%=7.3g,由标签中浓盐酸的溶质的质量分数36.5%,根据溶质的质量分数=溶质的质量/溶液的质量 ×100%,则:
这种浓盐酸溶液的质量=溶质的质量/溶质的质量分数 =7.3g /36.5% =20g,
根据m=ρV,V浓盐酸=m/ρ=20g/ 1.18g/cm3 =16.95cm3=16.9mL;
②由于①计算这种稀盐酸中溶质的质量为7.3g,设最多可得氢气的量为m,根据题意得:
Zn+2HCl=ZnCl2+H2↑
73 2
7.3g m
73 /7.3g =2 /m m=0.2g


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:2012年苏州市草桥中学初三二模化学试卷(带解析) 题型:计算题
(3分)下图是浓盐酸试剂瓶标签的部分内容。请回答:
① 欲配制200g溶质质量分数为3.65%的稀盐酸,需要这种浓盐酸 g,体积为 mL。
②用①中所得稀盐酸与足量锌粒反应,请根据化学方程式计算最多可得氢气的质量
查看答案和解析>>
科目:初中化学 来源:2012年苏州市初三二模化学试卷(解析版) 题型:计算题
(3分)下图是浓盐酸试剂瓶标签的部分内容。请回答:

① 欲配制200g溶质质量分数为3.65%的稀盐酸,需要这种浓盐酸 g,体积为 mL。
②用①中所得稀盐酸与足量锌粒反应,请根据化学方程式计算最多可得氢气的质量
查看答案和解析>>
科目:初中化学 来源:上海市模拟题 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:
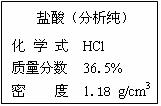
右图是浓盐酸试剂瓶标签的部分内容。请回答:
① 欲配制200g溶质质量分数为3.65%的稀盐酸,
需要这种浓盐酸 g,
体积为 mL。
② 用①中所得稀盐酸与足量锌粒反应,请根据化学方程式计算最多可得氢气的
质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com