
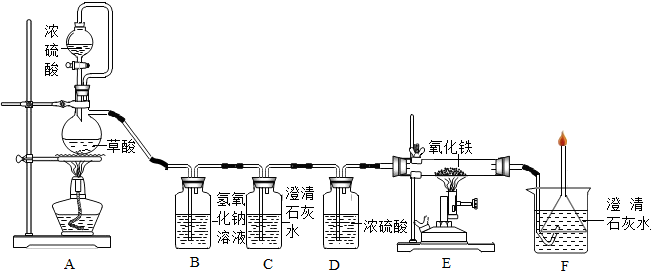
分析 (1)根据在B装置中氢氧化钠与二氧化碳反应生成了碳酸钠和水进行分析;
(2)根据澄清石灰水能检验二氧化碳的存在分析判断;
(3)根据浓硫酸具有很好的吸水性进行分析;
(4)根据一氧化碳还原氧化铁在高温的条件下生成铁和二氧化碳进行分析;
(5)从F装置中的溶液成分以及对尾气的处理分析即可;
(6)根据铁和盐酸反应生成氯化亚铁和氢气进行分析.
解答 解:(1)在B装置中氢氧化钠与二氧化碳反应生成了碳酸钠和水,化学方程式是:2NaOH+CO2═Na2CO3+H2O;
(2)C装置中的澄清石灰水遇二氧化碳变浑浊,而C装置中无明显现象,说明二氧化碳已被氢氧化钠溶液完全吸收;
(3)由于浓硫酸具有很好的吸水性,可用来干燥一氧化碳气体;
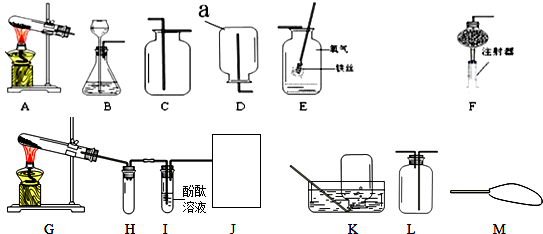
(4)在E装置中的氧化铁在CO的还原作用下,生成了铁和二氧化碳,所以实验的现象是:红色的氧化铁粉末变成黑色,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(5)①由澄清的石灰水变浑浊,检验一氧化碳与氧化铁反应后有二氧化碳气体生成;②利用燃烧法处理多余的一氧化碳气体,防止空气污染;
(6)生成氢气的质量为:11.5g+116.2g-127.3g=0.4g,
设参加反应的铁的质量为x,生成硫酸亚铁质量为y
Fe+2HCl=FeCl2+H2↑
56 127 2
x y 0.4g
$\frac{56}{x}$=$\frac{127}{y}$=$\frac{2}{0.4g}$
x=11.2g
y=25.4g
所以反应后所得溶液溶质的质量分数为:$\frac{25.4g}{127.3g+11.2g-0.4g}$×100%=18.4%.
故答案为:(1)2NaOH+CO2═Na2CO3+H2O;
(2)证明A装置中生成的二氧化碳已被B装置中的氢氧化钠溶液完全吸收;
(3)干燥一氧化碳气体;
(4)红色粉末变成黑色,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(5)证明一氧化碳与氧化铁反应生成了二氧化碳,燃烧未参加反应的一氧化碳,防止其污染空气;
(6)18.4%.
点评 本题考查一氧化碳还原氧化铁的实验装置及相关问题,属于课本基本实验的延伸,难度不大,要明确实验的目的及试剂的作用.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:选择题
| A. | 蜡烛燃烧,石蜡难溶于水 | |
| B. | 冰融化成水,水是无色无味的液体 | |
| C. | 钢铁生锈,氧气具有氧化性 | |
| D. | 干冰升华,CO2能使澄清石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
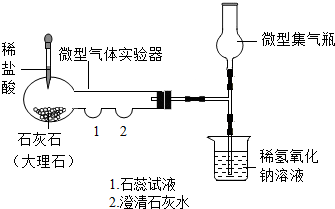 如图是二氧化碳的制取和性质实验的微型一体化装置图,该装置的气密性良好.请回答下列问题:
如图是二氧化碳的制取和性质实验的微型一体化装置图,该装置的气密性良好.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
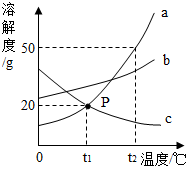 如图是a、b、c三种物质的溶解度曲线,据图回答:
如图是a、b、c三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只能用固体氯化钠和水配制 | |
| B. | 量液时,仰视会导致实际液体值偏小 | |
| C. | 溶解过程中玻璃棒的作用是搅袢,加快溶解 | |
| D. | 称量氯化钠时把药品和砝码位置放反了导致称量结果偏大 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
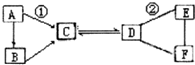 A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)
A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com