
分析 (1)富含蛋白质的食物由瘦肉类、蛋类、豆类、干果类等;(2)从人体所需的各种营养元素的生理作用方面分析;(3)三大合成材料:塑料、合成纤维、合成橡胶;(4)根据羊毛的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,进行分析判断.
解答 解:(1)鸡蛋属于蛋类,鸡蛋含丰富的优质蛋白质;
(2)钙是构成人体骨胳的主要元素,幼儿或青少年缺钙,可能导致佝偻病;
(3)塑料水杯是用塑料制成的,塑料属于三大合成材料之一,属于合成材料;
(4)羊毛的主要成分是蛋白质,燃烧时有烧焦羽毛的气味,腈纶没有,可用燃烧法区别腈纶和羊毛.
故答案为:(1)鸡蛋;(2)钙;(3)塑料水杯;(4)燃烧.
点评 本题难度不大,掌握羊毛纤维与合成纤维的鉴别方法(灼烧闻气味)是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
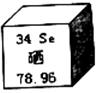 硒元素具有抗衰老、抑制癌细胞的功能.硒元素在元素周期表中有如图所示信息.下列有关说法不正确的是( )
硒元素具有抗衰老、抑制癌细胞的功能.硒元素在元素周期表中有如图所示信息.下列有关说法不正确的是( )| A. | 硒属于金属元素 | B. | 硒的原子核内有34个质子 | ||
| C. | 硒的相对原子质量为78.96 | D. | 富硒食品可以预防癌症 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4、BaCl2、KNO3、NaCl | B. | K2CO3、BaCl2、Na2CO3、HCl | ||
| C. | KOH、Na2SO4、CuSO4、MgCl2 | D. | NaNO3、AgNO3、KNO3、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com