
| A. | 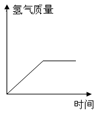 | B. | 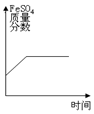 | C. |  | D. |  |
分析 往一定量的稀硫酸中加入过量的铁粉,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,由于稀硫酸是一定量的,铁粉是过量的,最终稀硫酸完全被消耗,据此进行分析判断.
解答 解:A、往一定量的稀硫酸中加入过量的铁粉,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,至完全反应,氢气的质量不再增加,选项图象与反应过程相符,故选项正确.
B、往一定量的稀硫酸中加入过量的铁粉,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,反应前没有硫酸亚铁,故图象应从原点开始,选项图象与反应过程不相符,故选项错误.
C、往一定量的稀硫酸中加入过量的铁粉,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,反应后酸性变弱,pH应增大,选项图象与反应过程不相符,故选项错误.
D、往一定量的稀硫酸中加入过量的铁粉,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,由于稀硫酸是一定量的,铁粉是过量的,最终铁的质量不可能为0,选项图象与反应过程不相符,故选项错误.
故选:A.
点评 本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.


科目:初中化学 来源: 题型:选择题
| A. | 氧气是由氧元素组成的,所以制取氧气的反应物中一定含有氧元素 | |
| B. | 感应电流是由导体切割磁感线产生的,所以导体切割磁感线就一定能产生感应电流 | |
| C. | 可燃物的燃烧时温度必须达到着火点,所以温度达到了着火点,可燃物就能燃烧 | |
| D. | 单质中只含有一种元素,所以只含一种元素的物质一定是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KCl | B. | Ca(H2PO4)2 | C. | (NH4)2SO4 | D. | KNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2.4克 | B. | 5克 | C. | 6克 | D. | 4.8克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com