
【题目】某不纯的烧碱样品中含有Na2CO33.8%、Na2O5.8%、 NaOH90.4%, 取M克样品,溶于质量分数为14.6%的盐酸溶液100克中,并用30%的NaOH溶液来中和剩余的盐酸至中性.把反应后的溶液蒸干后可得到固体质量为( )
A.23.4g
B.30.6g
C.35.7g
D.58.5g
科目:初中化学 来源: 题型:
【题目】图1表示甲、乙两种晶体的溶解度曲线。t1℃时,分别将20g甲、乙两种晶体(不含结晶水)加入盛有100g水的两个烧杯中,恰好完全溶解;升温到t2℃时,两烧杯中出现图2所示的现象。下列说法不正确的是
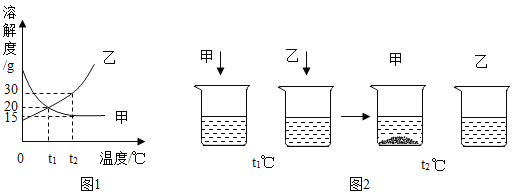
A.t2℃时烧杯中乙物质形成的溶液是不饱和溶液
B.t2℃时烧杯中甲物质溶液溶质质量分数约为15%
C.若改变温度,必须降温至t1℃以下才能将t2℃烧杯中甲的溶液转变为不饱和溶液
D.将t1℃时两烧杯中的溶液分别升温到t2℃时,所得溶液溶质质量分数甲<乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组将Cu块加入到盛稀H2SO4溶液的试管中,Cu 块不溶解,不发生化学反应。再向此试管中加入KNO3溶液,发现Cu块逐渐溶解,有无色气体产生,该气体与空气接触后变成红棕色的气体,最后Cu块完全溶解,变成蓝色溶液。
[提出问题] Cu块与什么物质发生了化学反应,产生的气体是H2吗?
小军同学认为产生的气体一定不是 H2,你认为他作出此判断的合理理由是_________________。
[查阅资料]他们通过查阅资料知道: NO 是一种无色气体,与空气接触后生成红棕色的NO2气体。请写出此气体颜色发生变化的化学方程式________________。
[提出猜想]
猜想一: Cu块与KNO3溶液发生了化学反应;
猜想二: Cu块与K2SO4溶液发生了化学反应;
猜想三: Cu块与_______溶液发生了化学反应。
[设计实验]
实验步骤 | 实验现象 | 解释或结论 |
①将Cu块加入KNO3溶液中。 | Cu块不溶解 | 说明猜想一是错误的 |
②将Cu块加入到______溶液中 | Cu块不溶解 | 说明猜想二是错误的 |
③将Cu块加入到稀HNO3溶液中 | Cu块溶解,有无色气体产生,该气体与空气接触后变成红棕色的气体,溶液变成蓝色 | 说明猜想三是正确的 |
[实验结论]猜想三成立。该反应的化学方程式为![]() _________+_____________。
_________+_____________。
[讨论交流]实验结束后,同学们在一起进行交流。从复分解反应的角度分析,H2SO4和KNO3_____________。(填“能”或“不能”)发生化学反应。Cu块是如何与稀HNO3溶液发生化学反应的呢?他们带着这个问题去请教老师,老师告诉他们:H2SO4溶液解离出H和SO42-,KNO4溶液解离出_____, 可以间接地看成有HNO3 溶液。老师还告诉大家: Ag也能与稀HNO3溶液反应。请写出将Ag粉加入到HCl和NaNO3混合溶液中所产生的实验现象_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学欲测定草木灰中碳酸钾的含量,称取 69g 试样于烧杯中,加入 29.2g 稀盐酸恰好完全反应,反应后,称得烧杯内混合物的总质量为 93.8g(忽略二氧化碳的溶解对质量的影响)。(可能发生的反应有:K2CO3+2HCl=2KCl+H2O+CO2↑)请计算:
(1)反应过程中产生的二氧化碳质量为_____g。
(2)该草木灰试样中碳酸钾的质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了防上污染,用黄铜矿(主要皮分是CuFeS2及少量含Zn的化合物)炼铜时,将产生的废气、废液转换成工业原料,设计流程如下:

(1)已知步骤①为化合反应且反应前后各元素的化合价均不变,则X的化学式为_____。
(2)写出步骤②中反应的化学方程式_____。(任写一个)
(3)步骤③的操作是_____,固体B的化学式为_____。
(4)写出固体D的一种用途:_____,滤液a和b中相同溶质的名称为_____。
(5)若操作过程中物质的损失忽略不计,要生成2.8g B和3.2gD,则加入Zn的质量应大于_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现探究一固体混合物的成分,已知其中可能含有Na2CO3、CuSO4、 BaCl2、 K2SO4、 NaCl 五种物质中的一种或几种,按图所示进行实验操作,出现的现象如图中所述(设过程中所有可能发生的反应都完全进行)

试根据实验过程和发生的现象做出判断,完成下列问题:
(1)根据操作①所得现象,则物质中一定没有_____。
(2)根据操作②所得现象,则物质中一定含有_____,一定没有_____。
(3)根据操作③所得现象,则物质中一定有_____。
(4)通过实验操作④所得滤液中,一定含有的阳离子是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列溶解度曲线和A物质的部分温度是的溶解度判断下列说法正确的是( )
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | A物质 | 20 | 28 | 45 | 60 |
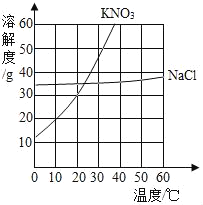
A. 由上图可知,KNO3和NaCl的溶解度均大于A 物质的溶解度
B. 10℃时,将40gNaCl放入50g水中,充分溶解,所得溶液是NaCl的不饱和溶液
C. 将30℃时NaCl、KNO3、和A物质的饱和溶液各降温至10℃,所得溶液的溶质质量分数大小为:KNO3>NaCl>A
D. 20℃时,将KNO3、NaCl和A物质各30g分别配制成恰好饱和溶液,所得溶液的质量大小为A>KNO3=NaCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了以下四个实验方案,理论上正确,操作上可行,经济上合理的是( )
A.Cu![]() CuCl2
CuCl2![]() Cu(OH)2
Cu(OH)2
B.H2O![]() O2
O2![]() MgO
MgO
C.CaCO3![]() CaO
CaO![]() Ca(OH)2
Ca(OH)2![]() NaOH溶液
NaOH溶液
D.MgCl2![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亮亮同学做镁条在空气中燃烧的实验时,发现镁条燃烧除生成白色固体(MgO)外,还有少量的淡黄色固体生成。这种淡黄色固体是什么呢?亮亮在老师的指导下进行有关实验探究:
(实验探究)将该淡黄色固体投入到盛有水的烧杯中。
(实验现象)在该淡黄色固体与水反应的烧杯中产生了白色沉淀,并有刺激性气味的气体逸出。
(教师指导)上述反应产生的白色沉淀为Mg(OH)2,生成的气体为NH3,反应过程中每种元素的化合价在反应前后都不发生改变。
(问题解决)此淡黄色固体中肯定含有镁元素和____元素,判断的依据是__,若该物质仅由两种元素组成,其化学式为____,此物质与水反应的化学方程式为____。
(相关结论)空气中氮气(N2)和氧气(O2)的体积比约为______,氮气在空气中的含量远远多于氧气,但镁条在空气中燃烧只生成少量的淡黄色固体,由此得出的一个结论是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com