
”¾ĢāÄæ”æĻĀĮŠ»ÆѧÓĆÓļŹéŠ“ÕżČ·µÄŹĒ
A. 2 øöĀČŌ×Ó£ŗCl2
B. 3 øöŅ»Ńõ»ÆµŖ·Ö×Ó£ŗ3NO
C. 5 øöĢśĄė×Ó£ŗ5Fe2+
D. Ńõ»ÆĆ¾ÖŠĆ¾ŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ£«2¼Ū£ŗ![]()
”¾“š°ø”æB
”¾½āĪö”æ
A”¢øł¾ŻŌ×ӵıķŹ¾·½·Ø£ŗÓĆŌŖĖŲ·ūŗÅĄ“±ķŹ¾Ņ»øöŌ×Ó£¬±ķŹ¾¶ąøöøĆŌ×Ó£¬¾ĶŌŚĘäŌŖĖŲ·ūŗÅĒ°¼ÓÉĻĻąÓ¦µÄŹż×Ö£¬Ōņ2øöĀČŌ×Ó![]() £¬¹ŹA²»ÕżČ·£»
£¬¹ŹA²»ÕżČ·£»
B”¢·Ö×ӵıķŹ¾·½·Ø£ŗÕżČ·ŹéŠ“ĪļÖŹµÄ»ÆѧŹ½£¬±ķŹ¾¶ąøöøĆ·Ö×Ó£¬¾ĶŌŚĘä»ÆѧŹ½Ē°¼ÓÉĻĻąÓ¦µÄŹż×Ö£¬Ōņ3øöŅ»Ńõ»ÆµŖ·Ö×Ó![]() £¬¹ŹBÕżČ·£»
£¬¹ŹBÕżČ·£»
C”¢øł¾ŻĄė×ӵıķŹ¾·½·Ø£ŗŌŚ±ķŹ¾øĆĄė×ÓµÄŌŖĖŲ·ūŗÅÓŅÉĻ½Ē£¬±ź³öøĆĄė×ÓĖł“ųµÄÕżøŗµēŗÉŹż£¬Źż×ÖŌŚĒ°£¬Õżøŗ·ūŗÅŌŚŗ󣬓ų1øöµēŗÉŹ±£¬1ŅŖŹ”ĀŌ£¬Ōņ5øöĢśĄė×Ó![]() £¬¹ŹC²»ÕżČ·£»
£¬¹ŹC²»ÕżČ·£»
D”¢ÓÉ»ÆŗĻ¼ŪµÄ±ķŹ¾·½·Ø£¬ŌŚøĆŌŖĖŲµÄÉĻ·½ÓĆÕżøŗŗÅŗĶŹż×Ö±ķŹ¾£¬ÕżøŗŗÅŌŚĒ°£¬Źż×ÖŌŚŗó£¬Ńõ»ÆĆ¾ÖŠĆ¾ŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ£«2¼Ū£ŗ![]() £¬¹ŹD²»ÕżČ·”£¹ŹŃ”B”£
£¬¹ŹD²»ÕżČ·”£¹ŹŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ÉÕ±ÖŠŹ¢ÓŠ22.3æĖĢ¼ĖįÄĘŗĶĀČ»ÆÄĘ×é³ÉµÄ¹ĢĢå»ģŗĻĪļ£¬¼Ó×ćĮæĖ®Čܽā£¬ÖĘ³ÉČÜŅŗ£®ĻņĘäÖŠÖš½„µĪ¼ÓČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĻ”ŃĪĖį£¬·Å³öĘųĢåµÄ×ÜÖŹĮæÓėĖłµĪČėĻ”ŃĪĖįµÄÖŹĮæ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£ŗ
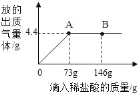
£Ø1£©µ±µĪ¼ÓĮĖ73æĖĻ”ŃĪĖįŹ±£¬·Å³öĘųĢåµÄ×ÜÖŹĮæĪŖ_____æĖ£®
£Ø2£©µ±µĪ¼ÓĻ”ŃĪĖįÖĮĶ¼ÖŠBµćŹ±£¬ÉÕ±ÖŠČÜŅŗĄļµÄČÜÖŹŹĒ£ØŠ“»ÆѧŹ½£©_____”£
£Ø3£©µ±µĪ¼ÓĮĖ73æĖĻ”ŃĪĖįŹ±£Ø¼“Aµć£©£¬ÉÕ±ÖŠĪŖ²»±„ŗĶČÜŅŗ£¬ŹŌĶعż¼ĘĖćĒó³öĘäÖŠČÜÖŹµÄÖŹĮæ·ÖŹż£®_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖ²ā¶Ø±źÓŠÖŹĮæ·ÖŹżĪŖ32%µÄŃĪĖįµÄŹµ¼ŹÖŹĮæ·ÖŹż£¬Š”Ć÷ŹµŃ鏱ĻČŌŚÉÕ±ÖŠ¼ÓČė20 g 40%µÄĒāŃõ»ÆÄĘČÜŅŗ£¬ŌŁÖšµĪ¼ÓČėøĆŃĪĖį£¬²ā¶Ø³ö¼ÓČėŃĪĖįµÄÖŹĮæÓėÉÕ±ÖŠČÜŅŗpHµÄ¹ŲĻµČēĶ¼”£
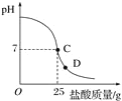
(1)ĖłÓĆĒāŃõ»ÆÄĘČÜŅŗÖŠČÜÖŹµÄÖŹĮæĪŖ_____g”£
(2)ĒėČĻÕęæ“ĒåÉĻĶ¼ŠÅĻ¢ŗó»Ų“šŅŌĻĀĪŹĢā”£
¢Łµ±µĪ¼ÓŃĪĖįµ½CµćŹ±£¬ĖłĻūŗĵÄŃĪĖįÖŠČÜÖŹµÄÖŹĮæŹĒ¶ąÉŁ£æ_____”£
¢ŚøĆŃĪĖįµÄŹµ¼ŹÖŹĮæ·ÖŹżŹĒ¶ąÉŁ£æ(±£Įōµ½0.1%)_____”£
¢Ūµ¼ÖĀŃĪĖįČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹżøıäµÄŌŅņŹĒ_____”£
¢Üµ±µĪ¼ÓŃĪĖįµ½Ķ¼ĻńÖŠDµćŹ±£¬ÉÕ±ÖŠČÜŅŗµÄČÜÖŹŹĒ_____(Ģī»ÆѧŹ½)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢CČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾”£
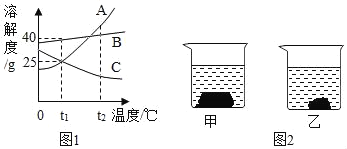
£Ø1£©µ±ČżĪļÖŹČܽā¶Č“óŠ”ĪŖB£¾C£¾AŹ±£¬ĪĀ¶ČtµÄ·¶Ī§ŹĒ_____”£
£Ø2£©t2”ꏱ£¬½«A”¢B”¢Cø÷25g·Ö±š·ÅČė100gĖ®ÖŠ£¬ÄÜŠĪ³É±„ŗĶČÜŅŗµÄĪļÖŹŹĒ_____£¬¶ųƻӊŠĪ³É±„ŗĶČÜŅŗµÄ£¬æɽ«ČÜŅŗĪĀ¶Č½µµ½t1”ꏱ£¬ÓÖÄÜĒ”ŗĆŠĪ³É±„ŗĶČÜŅŗµÄŹĒ_____”£
£Ø3£©t2”ꏱ£¬½«µČÖŹĮæµÄA”¢B”¢CČżÖÖĪļÖŹ¼ÓŹŹĮæµÄĖ®·Ö±šŠĪ³É±„ŗĶČÜŅŗ£¬ČżÖÖ±„ŗĶČÜŅŗÖŠŗ¬Ė®µÄÖŹĮæÓɓ󵽊”µÄĖ³ŠņĪŖ_____£ØÓĆA”¢B”¢C±ķŹ¾£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøß“æ¶ČµÄµ„¾§¹čŹĒÖĘ×öµē×ӼƳɵēĀ·µÄ»ł“”²ÄĮĻ”£¹¤ŅµÉĻÖʱøøß“æ¹čµÄ»Æѧ·“Ó¦ŌĄķĪŖ£ŗ
¢ŁSiO2+2C![]() Si +2CO”ü”¢¢ŚSi+3HCl
Si +2CO”ü”¢¢ŚSi+3HCl![]() HSiCl3+H2”¢¢ŪHSiCl3+H2
HSiCl3+H2”¢¢ŪHSiCl3+H2![]() Si+3X£¬·“Ó¦¢ŁÖĘµĆ“Ö¹č£¬Ķعż·“Ó¦¢Ś¢Ū½ųŅ»²½µĆµ½øß“æ¹č£»ČżĀČ¹čĶé(HSiCl3)µÄ·ŠµćŹĒ31.8”ę”£ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ
Si+3X£¬·“Ó¦¢ŁÖĘµĆ“Ö¹č£¬Ķعż·“Ó¦¢Ś¢Ū½ųŅ»²½µĆµ½øß“æ¹č£»ČżĀČ¹čĶé(HSiCl3)µÄ·ŠµćŹĒ31.8”ę”£ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ
A. ·“Ó¦¢ŪÖŠXµÄ»ÆѧŹ½ĪŖHCl
B. ČżĀČ¹čĶéÓÉĒā”¢¹č”¢ĀČČżÖÖŌŖĖŲ×é³É
C. ČżĀČ¹čĶéÖŠ¹č”¢ĀČŌŖĖŲµÄÖŹĮæ±ČĪŖ1”Ć3
D. ·“Ó¦¢Ś¢ŪŹµĻÖĮĖ¹čŌŖĖŲµÄø»¼Æ£¬½«“Ö¹č×Ŗ»ÆĪŖøß“æ¹č
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧĶŲÕ¹æĪĢƵÄÖ÷ĢāŹĒ£ŗĢ½ĆŲĀČ»ÆÄĘѳʷ”£
Ö÷Ģā¢ń Ģ½¾æĀČ»ÆÄĘѳʷ֊ŌÓÖŹµÄ³É·Ö
ŅŃÖŖĖłĢį¹©µÄĀČ»ÆÄĘѳʷ֊£¬æÉÄÜŗ¬ÓŠĮņĖįÄĘ”¢ĀČ»ÆĆ¾”¢ĀČ»ÆøĘÖŠµÄŅ»ÖÖ»ņ¼øÖÖŌÓÖŹ”£¼×Ķ¬Ń§µÄŹµŃéĢ½¾æ¹ż³Ģ¼ĒĀ¼ČēĻĀ£ŗ
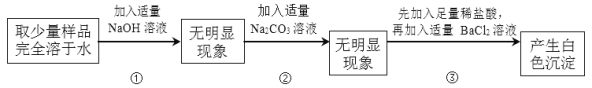
øł¾ŻŅŌÉĻŹµŃéŠÅĻ¢£¬¼×Ķ¬Ń§µĆ³ö½įĀŪ£ŗ“ĖĀČ»ÆÄĘѳʷ֊ŗ¬ÓŠµÄŌÓÖŹŹĒĮņĖįÄĘ”£
£ØŹµŃé·ÖĪö£©
£Ø1£©²½Öč¢ŁÖŠ¼ÓČėŹŹĮæNaOH ČÜŅŗµÄÄæµÄŹĒ_____”£
£Ø2£©ŅŅĶ¬Ń§ČĻĪŖ²½Öč¢ŪÖŠ²»ŠčŅŖ¼ÓČė×ćĮæĻ”ŃĪĖį£¬ÄćŹĒ·ńĶ¬ŅāĖūµÄ¹Ūµć£æ_____£ØŃ”Ģī”°Ķ¬Ņā”±»ņ”°²»Ķ¬Ņā”±£©£¬ĒėĖµĆ÷ŌŅņ_________”£
Ö÷Ģā¢ņ ²ā¶ØĀČ»ÆÄĘѳʷ֊ĀČ»ÆÄʵÄÖŹĮæ·ÖŹż
Č·¶ØĮĖĀČ»ÆÄĘѳʷ֊ŌÓÖŹµÄ³É·Öŗ󣬼×Ķ¬Ń§¶Ōѳʷ֊ĀČ»ÆÄʵÄÖŹĮæ·ÖŹż½ųŠŠ²ā¶Ø”£³ĘČ”20.0g ĀČ»ÆÄĘѳʷӌÉÕ±ÖŠ£¬¼Ó×ćĮæµÄĖ®³ä·ÖČܽā£¬ŌŁĻņĘäÖŠ¼ÓČėĀČ»Æ±µČÜŅŗÖĮ²»ŌŁ²śÉś³ĮµķĪŖÖ¹£¬³Įµķ¾¹żĀĖ”¢Ļ“µÓ”¢øÉŌļŗó³ĘĮ棬ĘäÖŹĮæĪŖ 2.33g”£øĆѳʷ֊ĀČ»ÆÄʵÄÖŹĮæ·ÖŹżŹĒ_____”££ØŠ“³ö¼ĘĖć²½Öč£¬¼ĘĖć½į¹ū¾«Č·µ½ 0.1%£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(9·Ö)ÕÅ»ŖĶ¬Ń§¶ŌĖį”¢¼ī”¢ŃĪµÄÖŖŹ¶½ųŠŠĮĖŅŌĻĀµÄŹįĄķ”£
£Ø1£©ĢīŠ“ĻĀ±ķæÕøńÖŠµÄ»ÆѧŹ½”£
ĀČ»Æ¼Ų | ĀČ»ÆøĘ | ĀČ»ÆÄĘ | ĀČ»ÆĆ¾ | ĀČ»ÆĀĮ | ĀČ»ÆŠæ | ĀČ»ÆŃĒĢś | ĀČ»ÆĶ |
KCl | CaCl2 | NaCl | MgCl2 | ZnCl2 | FeCl2 |
Ė¼æ¼£ŗøł¾ŻŅŌÉĻŃĪÖŠµÄ½šŹōŌŖĖŲµÄÅÅĮŠ£¬æÉŅŌµĆ³öĖūŹĒŅĄ¾Ż______________Ė³Šņ¹éÄÉÕūĄķµÄ”£
£Ø2£©ĪŖĄķ½āĻ”ŃĪĖįŗĶĒāŃõ»ÆÄĘĮ½ÕßÖ®¼ä·¢Éś·“Ó¦µÄĪ¢¹ŪŹµÖŹ£¬»ęÖĘĮĖČēĶ¼”£ĒėÄćŌŚÓŅ±ßµÄŌ²Č¦ÖŠĢīČėŹŹµ±µÄ»ÆѧŹ½»ņĄė×Ó·ūŗÅ£ŗ

£Ø3£©ÕÅ»ŖĶ¬Ń§·¢ĻÖĖį”¢¼ī”¢ŃĪÖ®¼äµÄ·“Ó¦¶¼ÓŠŃĪĄąĪļÖŹÉś³É”£ĒėŠ“³öŅ»øöÄÜÉś³ÉMgCl2µÄø“·Ö½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ__________________________”£
£Ø4£©ĪŅĆĒÖŖµĄČÜŅŗĖį¼ī¶ČpHæÉĻŌŹ¾µÄČÜŅŗµÄĖį¼īŠŌ£»ĖįČÜŅŗpH£¼7£¬ČÜŅŗĻŌĖįŠŌ£»¼īČÜŅŗpH£¾7£¬ČÜŅŗĻŌ¼īŠŌ£®Ģį³öĪŹĢā£ŗŃĪČÜŅŗµÄpHŌõŃłÄŲ£æŃĪČÜŅŗĻŌŹ²Ć“ŠŌÄŲ£æ
²ĀĻėÓė¼ŁÉč£ŗŃĪČÜŅŗµÄpHæÉÄÜĪŖ£ŗpH=7”¢pH£¼7”¢pH£¾7£®
Éč¼ĘÓėŹµŃé£ŗĻĀĮŠŹĒĮ½Ķ¬Ń§·Ö±š¶ŌĻąĶ¬µÄNaClČÜŅŗ”¢CuSO4ČÜŅŗ”¢K2CO3ČÜŅŗµÄpH½ųŠŠµÄ²ā¶ØŹµŃé£ŗ¼×Ķ¬Ń§£ŗČ”pHŹŌÖ½·ÅŌŚ²£Ę¬ÉĻ£¬ÓĆ²£°ōÕŗČ”²āŹŌŅŗµĪŌŚpHŹŌÖ½ÉĻ£¬ŹŌÖ½ĻŌÉ«ŗóÓėpH±ź×¼±ČÉ«æØ±Č½Ļ£®ŅŅĶ¬Ń§£ŗČ”pHŹŌÖ½·ÅŌŚ²£Ę¬ÉĻ£¬ÓĆÕōĮóĖ®½«pHŹŌÖ½ČóŹŖ£¬ŌŁÓĆ²£°ōÕŗČ”²āŹŌŅŗµĪŌŚpHŹŌÖ½ÉĻ£¬ŹŌÖ½ĻŌÉ«ŗóÓėpH±ź×¼±ČÉ«æØ±Č½Ļ£®
¼ĒĀ¼Źż¾Ż£ŗĻĀ±ķŹĒĮ½Ķ¬Ń§¼ĒĀ¼Ėł²āpHµÄŹµŃ鏿¾Ż£ŗ
NaClČÜŅŗ | CuSO4ČÜŅŗ | K2CO3ČÜŅŗ | |
¼×Ķ¬Ń§ | 7 | 4 | 10 |
ŅŅĶ¬Ń§ | 7 | 5 | 9 |
½įĀŪ£ŗĶعż²ā¶Ø¼øÖÖŃĪČÜŅŗµÄpH£¬æÉŅŌµĆ³öµÄ½įĀŪŹĒ£ŗ £®
ĘĄ¼ŪÓė·“Ė¼£ŗÉĻŹöĮ½Ķ¬Ń§²āµĆµÄŹż¾Ż£¬·“Ó³ĮĖČÜŅŗÕꏵpHµÄŹĒ Ķ¬Ń§”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²Ł×÷£¬ÄÜ“ļµ½Ō¤ĘŚÄæµÄŹĒ
¢ŁÓĆĶŠÅĢĢģĘ½³ĘČ”5.6gCuO·ŪÄ©
¢ŚÓĆ10mLĖ®ŗĶ10mL¾Ę¾«ÅäÖĘ20mL¾Ę¾«ČÜŅŗ
¢Ū½«50gČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĻ”ŃĪĖį¼ÓČČÕō·¢µō25gĖ®£¬µĆµ½ČÜÖŹÖŹĮæ·ÖŹżĪŖ20%µÄŃĪĖį
¢ÜÓĆ10mLµÄĮæĶ²Č”8.2mLĖ®
A£®¢Ł¢Ū¢Ü B£®¢Ł¢Ü C£®¢Ł¢Ś¢Ü D£®¢Ś¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”抔Ć÷¶ŌĢśµÄŠāŹ“½ųŠŠČēĻĀĢ½¾æ£¬ŹŅĪĀŹ±£¬½«°üӊѳʷµÄĀĖÖ½°üÓĆ“óĶ·Õė¹Ģ¶ØŌŚĻš½ŗČūÉĻ£¬ŃøĖŁČū½ō£¬×°ÖĆČēĶ¼£¬¹Ū²ģµ½ĮæĶ²ÄŚĖ®ŃŲµ¼¹ÜĀżĀż½ųČė¹ćæŚĘæ£Ø¾»ČŻ»żĪŖ146mL£©”£µ±ĪĀ¶Č»Öø“ÖĮŹŅĪĀ£¬ĒŅĮæĶ²ÄŚĖ®Ćęøß¶Č²»±äŹ±¶ĮŹż£Ø“ĖŹ±ĘæÄŚŃõĘųŗ¬Įæ½üĖĘĪŖĮć£©”£¼ĒĀ¼ĘšŹ¼ŗĶ×īÖÕĮæĶ²µÄ¶ĮŹżŅŌ¼°ĖłŠčŹ±¼äČē±ķ”£
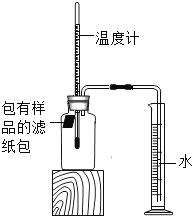
ŠņŗÅ | ѳʷ | ĮæĶ²ĘšŹ¼ ¶ĮŹż/mL | ĮæĶ²×īÖÕ ¶ĮŹż/mL | ĖłŠčŹ±¼ä /min |
1 | 1gĢś·Ū”¢0.2gĢ¼ŗĶ10µĪĖ® | 100 | 70 | Ō¼120 |
2 | lgĢś·Ū”¢0.2gĢ¼”¢10µĪĖ®ŗĶÉŁĮæNaCl | 100 | 70 | Ō¼70 |
3 | ”” | 100 | 70 | Ō¼480 |
£Ø1£©ŹµŃé¢ŁŗĶ¢ŚĖµĆ÷NaClæÉŅŌ_____ĢśŠāŹ“µÄĖŁĀŹ”£
£Ø2£©ŹµŃéæŖŹ¼ŗ󣬹ćæŚĘæÄŚĪĀ¶ČÓŠĖłÉĻÉż£¬ĖµĆ÷ĢśµÄŠāŹ“¹ż³ĢŹĒ_____£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©¹ż³Ģ”£
£Ø3£©ŹµŃé½įŹųŗóČ”³öĀĖÖ½°ü£¬¹Ū²ģµ½ÓŠŗģ×ŲÉ«ĪļÖŹÉś³É£¬øĆĪļÖŹµÄ»ÆѧŹ½ŹĒ_____”£
£Ø4£©ŅŃÖŖŗ¬Ģ¼Äܹ»¼ÓæģĢśµÄÉśŠāĖŁ¶Č£¬Š”Ć÷ĻėĶعżŹµŃé¢ŁŗĶ¢ŪŹĒĢ½¾æĢ¼¶ŌĢśŠāŹ“ĖŁĀŹµÄÓ°Ļģ£¬ĒėŌŚ±ķøńæհד¦ĢīŠ“ŹµŃé¢ŪµÄѳʷ×é³É_____”£
£Ø5£©øĆ×°ÖĆ»¹æÉÓĆÓŚ²āĮææÕĘųÖŠŃõĘųµÄŗ¬Į棬øł¾ŻÉĻŹöŹż¾Ż¼ĘĖćŃõĘųµÄĢå»żŗ¬ĮæŹĒ_____£ØŠ”Źżµćŗó±£Įō1Ī»£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com