
分析 【讨论猜想】(1)根据实验中所出现的现象,利用所掌握的基础知进行分析,评价小王的想法;
(2)小张的想法二:根据对其猜想中元素与反应前元素的对比,推断其猜想的理论依据;
【探究实验一】(1)结合猜想中的气体,对实验中现象进行分析,对气体组成做出判断;
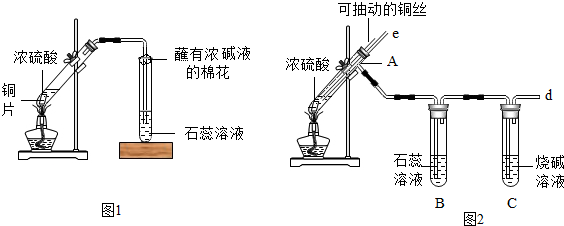
(2)观察装置中蘸有浓碱液的棉花的放置位置,利用碱液的性质,对其作用进行推断;
(3)对比两者的主要差别分析对结果的影响
【探究实验二】
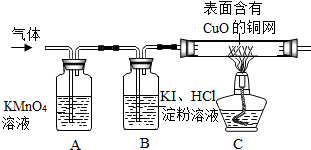
A、根据二氧化硫能使高锰酸钾溶液褪色的性质,预计实验现象,以说明气体中含有二氧化硫;
B、根据所提供的资料,判断若有氧气时会出现的实验现象,不含氧气时此现象不会出现;
C、根据氢气还原氧化铜的实验现象,推测不含氢气时所出现的现象;
【实验反思】根据探究的结论,铜可与浓硫酸发生反应,分析剩余溶液中硫酸的浓度变化,做出判断.
【实验结论】根据题目中信息,正确书写浓硫酸与Cu反应的化学反应方程式.
解答 解:【讨论猜想】(1)小王的想法一:实验中观察到放出稀硫酸的铜片无现象,说明铜片中不含活泼金属;
小王的想法二:实验中观察到溶液呈蓝色,说明有硫酸铜生成,因此铜一定参加了反应;
(2)小张的想法二:报猜想的气体的组成元素都是反应前物质中所含有的元素,因此可推测其猜想依据为:化学变化前后元素不变;
【探究实验一】(1)石蕊遇酸变红,观察到石蕊变红,说明气体遇水可形成酸性溶液,因此,判断气体中含有二氧化硫;
(2)利用二氧化硫能与碱溶液发生反应,放置于管口蘸有浓碱液的棉花吸收二氧化硫,防止造成空气污染;
(3)比较两实验装置,图2装置的优点是 通过抽动铜丝实现,能控制反应的发生与停止
【探究实验二】A、二氧化硫能使紫红色高锰酸钾溶液褪色,因此可观察到紫红色溶液逐渐褪色成无色;
B、不含有氧气,混合溶液就不能产生碘,因此淀粉溶液也就不会出现颜色变化;
C、不含氢气,灼热的氧化铜不能被还原,观察不到红色出现;
【实验反思】铜能与浓硫酸反应而与稀硫酸不能反应,随着反应的不断进行,溶液中硫酸的浓度逐渐减小,因此,停止反应后溶液中还会含有少量硫酸;
【实验结论】上述探究说明,所谓铜能与稀硫酸反应实际上是加热时水分蒸发、稀硫酸逐渐变成浓硫酸才与铜发生了反应.根据以上信息,则可以写出浓硫酸与Cu反应的化学反应方程式为Cu+2H2SO4=CuSO4+SO2+2H2O.
故答案为:
【讨论猜想】(1)如果含有活动性强的金属,加热前就应该冒气泡;
溶液变成蓝色,说明铜参加了反应;
(2)化学反应前后,元素的种类保持不变;
【探究实验一】(1)二氧化硫; (2)吸收多余的二氧化硫,防止污染空气;
(3)能控制反应的发生与停止;
【探究实验二】溶液褪色; 无明显现象; 无明显现象;
【实验结论】Cu+2H2SO4=CuSO4+SO2+2H2O.
点评 本题既涉及基础知识的运用,又涉及从信息中获取新知识并运用该知识分析问题,思维难度较大,处理时应注意知识的迁移与类比.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 :
:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| Mg(OH)2 | MgCO3 | |
| 溶解性 | 难溶于水 | 微溶于水 |
| 热稳定性 | 受热易分解,能生成两种氧化物 | 受热易分解,能生成两种氧化物 |
| 猜想 | 实验方法 | 现象 | 结论 | |
| ① | 二氧化碳 | 收集气体于集气瓶中,而后将气体通入澄清石灰水中; | 无明显现象 | 猜想①不成立 |
| ② | 氧气 | 收集气体于集气瓶中,而后将带火星的木条放入瓶中; | 无明显现象 | 猜想②不成立 |
| ③ | 氢气 | 第一步,点燃产生的气体; 第二步,在火焰上罩内壁涂有石灰水 的烧杯. | 气体能被点燃,产生蓝色火焰;烧杯内壁无现象; | 猜想③成立 |
| ④ | ||||
| ⑤ | 甲烷 | |||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不锈钢、焊锡、生铁是常见的合金 | |
| B. | 浓硫酸、纯碱、生石灰是常见的干燥剂 | |
| C. | 塑料、人造纤维、合成橡胶都是合成材料 | |
| D. | 蛋白质、纤维素、无机盐是常见的营养素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com