
| A. | 质量减少 | B. | 质量增加 | C. | 化学性质改变 | D. | 化学性质不变 |
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| H2O2的质量分数 | 反应现象 |
| 15% | 反应速度快,气体难以收集 |
| 10% | 反应比较平缓,导管口气流均匀、连续、易于收集,反应过程较易控制 |
| 5% | 反应平缓,导管口气流均匀、连续,易于收集 |
| 3% | 反应缓慢,需较长时间 |
| A. | 0%~3% | B. | 3%~5% | C. | 5%~10% | D. | 10%~15% |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 如图是某学校实验室从化学试剂商店买来的硫酸试剂的标签上的部分内容,请阅读后计算.欲配制500克溶质质量分数为19.6%的稀硫酸,
如图是某学校实验室从化学试剂商店买来的硫酸试剂的标签上的部分内容,请阅读后计算.欲配制500克溶质质量分数为19.6%的稀硫酸,查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗涤剂 乳化功能 清洗餐具 | B. | 酒精 可燃性 消毒剂 | ||
| C. | 干冰 升华吸热 人工降雨 | D. | 金刚石 硬度大 切割玻璃 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 该反应是化合反应 | |
| B. | 反应前后原子的种类、个数都不变 | |
| C. | 甲和丙两种物质的质量比为11:15 | |
| D. | 甲、乙、丙三种物质的分子数比为1:1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
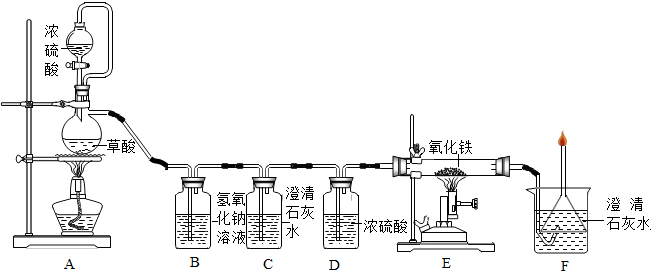
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
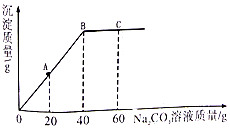 实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液,反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.已知:
实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液,反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.已知:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com