
【题目】如图1所示是氢氧化钠溶液与盐酸反应的实验研究。
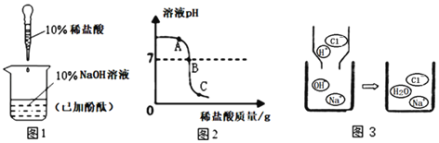
(1)随着盐酸不断滴入,烧杯中溶液的pH变化如图2所示,当滴加至A点时,烧杯中溶液呈_____色;溶液中的溶质是_____(填化学式);B点时恰好完全反应的化学方程式是_____。
(2)小明用微观示意图(图3)来说明反应的发生,请你从微观角度分析两者发生了化学反应的原因是_____。
【答案】红 NaOH、NaCl NaOH+HCl=NaCl+H2O 氢离子与氢氧根离子结合生成水
【解析】
(1)由图可知,滴加稀盐酸至A点时,溶液的pH>7,溶液显碱性,酚酞试液遇碱性溶液变红,故填红;
溶液显碱性,其中含有未反应的氢氧化钠,还有加入的稀盐酸遇与氧化钠反应生成的氯化钠,其化学式分别为NaOH、NaCl,故填NaOH、NaCl;
B点时氢氧化钠与盐酸恰好完全反应生成氯化钠和水,故反应的化学方程式写为:NaOH+HCl=NaCl+H2O。
(2)氢氧化钠属于碱,稀盐酸属于酸,氢氧化钠与盐酸发生了中和反应,该反应的微观实质是氢离子与氢氧根离子结合生成水,故填氢离子与氢氧根离子结合生成水。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:初中化学 来源: 题型:
【题目】A~J是初中化学常见的物质,A是一种含有四种元素的盐,可用作治疗胃酸过多,其反应原理:A和B反应生成C、D和E三种物质,通过光合作用D和E反应生成F和G,煤气主要成分H在F中燃烧生成E,I和D反应只生成J,J常用于改良酸性土壤。
(1)G的化学式为____,G中质量分数最大的元素是_________。
(2)A的俗称是____;A和B反应的化学方程式为___,基本反应类型是_____。
(3)I的用途是______(答1点即可);H在F中燃烧的化学方程式为___。
(4)改良后土壤浸出液的酸碱度可用_____测定。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:___,小王同学对“双氧水分解快慢的影响因素”进行了探究。
(提出问题)影响双氧水分解快慢的因素有哪些?
(猜想与假设)猜想一:可能与二氧化锰的形状有关;猜想二:可能与反应温度有关。
(设计并实验)小王同学用8ml3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2均有剩余):
实验编号 | 温度/℃ | 二氧化锰的形状(均取0.1g) | 收集到氧气的体积/ml(时间均为10s) |
① | 20 | 块状 | a |
② | 20 | 粉末状 | b |
③ | 20 | 块状 | c |
④ | 20 | 粉末状 | d |
(1)欲探究温度对“双氧水分解快慢”是否有影响,应该比较___和___(填“a”“b”“c”或“d”)的大小;若粉末状二氧化锰催化效果好,那么___>___(填“a”“b”“c”或“d”)。
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证:___。
(3)小王同学还使用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响,他在8mL 3%的双氧水中分别加入了0.03g、0.06g、0.08g、0.12g、0.24gMnO2,测得容器内压强的变化曲线如图所示(曲线的斜率代表征催化反应的速率),请你观察图示并写出两条规律性结论:

①___;
②___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有Fe2O3粉末的烧杯中加入过量的稀H2SO4,充分搅拌,粉末完全溶解;再向所得溶液中逐滴加入NaOH溶液,生成沉淀与加入NaOH溶液之间的质量关系如图所示。请回答下列问题:

(1)写出AB段内反应的化学方程式:_____。
(2)加入NaOH溶液40 g时溶液中存在的溶质是______(写化学式)。
(3)计算氢氧化钠溶液中溶质的质量分数。_____(要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-J是初中化学中常见的物质,其中A为气体,B为红棕色粉末,E为浅绿色溶液,G是一种建筑材料,它们之间的关系如图(部分反应物或生成物已略去)。
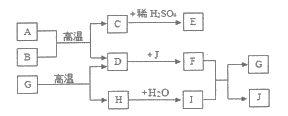
(1)写出化学式:E___________,H______________;
(2)A+B→C+D的化学反应方程式是_____________;
(3)F+I→G+J的化学反应方程式是____________;反应的基本类型为____________反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据如图回答问题:
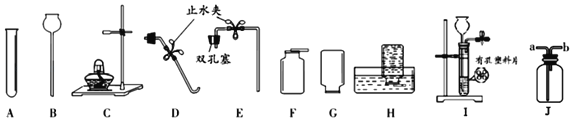
(1)写出下列仪器的名称:A_____,B_____。
(2)用KClO3与MnO2混合制取较纯净的O2,制取装置最好选用图中的_____(填字母,下同),收集时观察到_____时表明氧气已集满,上述制取氧气反应的化学方程式为_____。
(3)使用I装置制取二氧化碳,多孔隔板上放的药品名称应为_____。用该发生装置对比ABE组合装置,体现出的优点是_____。
(4)实验室常用硫化亚铁(FeS)固体和稀硫酸溶液,在常温下反应制取硫化氢(H2S)气体,制取硫化氢气体的化学方程式是_____;不用H装置收集H2S气体,说明H2S气体具有_____的物理性质;用J装置收集H2S气体应从_____(填“a”或“b”)端通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】瓦斯气的主要成分是CH4,存在煤矿坑道中。当煤矿坑道中瓦斯气达到一定浓度范围,遇明火就会发生爆炸,CH4与O2恰好完全反应时(生成CO2)爆炸最强烈。求煤矿坑道中瓦斯爆炸最强烈时CH4的体积百分含量(同温同压时,气体分子个数比等于其体积比)。
要求:写出计算过程,结果保留一位小数_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组利用混有少量CO2的CO气体还原氧化铜,并验证反应后的气体产物。
(1)请写出用一氧化碳还原氧化铜的化学方程式_____。
(2)实验室现有下图所示实验装置(可重复使用)。按气体从左到右的方向,装置连接顺序正确的是_____。
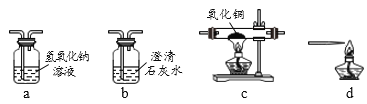
A b→c→a→b→d
B a→c→b→a→d
C a→b→c→b→d
D b→a→c→a→d
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2008年5月12日,我国汶川发生大地震.全国人民“众志成城,抗震救灾”.
(1)“拯救生命是第一位的”。为搜救埋在废墟下的幸存者,调用了许多搜救犬。搜救犬能根据人体发出的气味发现幸存者。从微观的角度分析搜救犬能发现幸存者的原因是____。
A 分子的质量很小 B 不同分子性质不同
C 分子不断运动 D 分子间有间隔
(2)地震中许多原有的水源被破坏。新水源需检测和处理后才能成为饮用水,我国规定水质必须在感官性指标、化学指标、病理学指标等方面均达标方可成为生活饮用水。
①感官性指标中有一项要求为:不得含有肉眼可见物,水应澄清透明。为达到此要求,净化水时,可以通过加入絮凝剂凝聚、沉降,然后通过__(填操作名称)而实现(见图)。图中还缺少的一种仪器是_,其作用是___。若过滤结束,发现滤液仍然浑浊,可能的原因是_(写一条)
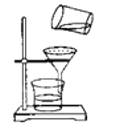
②化学指标中含有水源的pH和硬度两项。日常生活中用___区分硬水与软水.日常生活中使用硬水会带来许多麻烦,家庭生活中常用来降低水硬度的方法是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com