
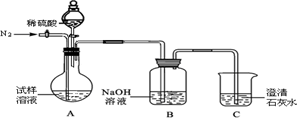
分析 (1)根据装置A中所加药品,利用药品间的反应规律,写出反应的化学方程式;
(2)根据实验的操作方法,理解实验的过程,分析实验过程中通入氮气所起到的作用及装置C中澄清石灰水在实验过程中的作用;
(3)对比稀硫酸与浓盐酸性质上的差异,分析若使用浓盐酸会对实验结果造成的影响;
(4)根据实验测得生成二氧化碳的质量,由反应的化学方程式计算出样品中碳酸钠的质量,而求得样品中碳酸钠的质量分数;
(5)利用碳酸钠的性质及变化规律,可使碳酸钠与氯化钙等形成沉淀等,另外设计实验进行碳酸钠质量分数的测定.
解答 解:
(1)样品中氯化钠不与硫酸反应,碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳,化学方程式为Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;
(2)为使残留在反应容器中生成的二氧化碳全部被氢氧化钠吸收,通入不能与氢氧化钠发生反应的氮气排出反应装置内的二氧化碳;装置C中盛放澄清石灰水检验二氧化碳气体是否全部被氢氧化钠吸收;
(3)稀硫酸不挥发而浓盐酸具有很强的挥发性,挥发出的HCl气体被氢氧化钠溶液吸收后,导致测得二氧化碳的质量偏高;
(4)氢氧化钠增重2.2g,说明反应放出2.2g二氧化碳,设反应消耗碳酸钠的质量为x
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
该样品中碳酸钠的质量分数=$\frac{5.3g}{5.5g}$×100%=96.4%
(5)碳酸钠能与氯化钙等反应生成碳酸钙沉淀,因此可选用氯化钙溶液与碳酸钠反应,通过测定生成沉淀或加入氯化钙的质量测定样品中碳酸钠的质量,而得到样品中碳酸钠的质量分数.碳酸钙与氯化钙反应的化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl.
故答案为:
(1)Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;
(2)排出装置A及导管中残留CO2,使其全部被装置B中NaOH溶液吸收;检验CO2是否被B瓶中的NaOH溶液完全吸收;
(3)偏高;
(4)96.4%;
(5)Na2CO3+CaCl2═CaCO3↓+2NaCl(或与BaCl2、Ba(OH)2反应).
点评 本题主要考查学生利用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


科目:初中化学 来源: 题型:选择题
| A. | Ba2+、H+、CO32- | B. | H+、OH-、Na+ | C. | Ag+、Cl-、NO3- | D. | Cu2+、Fe2+、SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 A、B、C是铁丝在氧气里燃烧的实验操作图,试回答下列问题:
A、B、C是铁丝在氧气里燃烧的实验操作图,试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com