
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
分析 化学反应的类型有四个:化合反应、分解反应、置换反应和复分解反应.化合反应是有两种或两种以上的物质生成一种物质的化学反应,特征是:多变一.分解反应是由一种物质生成两种或两种以上的物质的反应,特征是:一变多;置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的化学反应.复分解反应是两种化合物互相交换成分生成另外两种化合物的反应.古人将贝壳(主要成分是碳酸钙)灼烧后的固体,碳酸钙在高温的条件下生成氧化钙和二氧化碳,属于分解反应;氧化钙与水反应生成氢氧化钙,属于化合反应;氢氧化钙和碳酸钾反应生成氢氧化钾和碳酸钙白色沉淀,属于复分解反应.
解答 解:A、在上述反应过程中没有涉及的化学反应基本类型置换反应,故选项正确;
B、古人将贝壳(主要成分是碳酸钙)灼烧后的固体,碳酸钙在高温的条件下生成氧化钙和二氧化碳,属于分解反应;故选项错误;
C、氧化钙与水反应生成氢氧化钙,属于化合反应;故选项错误;
D、氢氧化钙和碳酸钾反应生成氢氧化钾和碳酸钙白色沉淀,属于复分解反应,故选项错误;
故选A
点评 本考点考查了基本反应类型的判断,要牢记四个基本反应类型的概念,并会理解应用.本考点基础性比较强,主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:实验探究题
| ①实验操作 | ②实验现象 |
| 剪下一片变黑的铜片,放入试管中, 通入足量的一氧化碳气体 | 铜片表面的黑色物质全部消失,露出红色的铜,将生成的气体通入澄清石灰水,石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na+、Cl、SO42-、Fe3+ | B. | SO42-、NO3-、K+、H+ | ||
| C. | Ba2+、Cl-、CO32-、K+ | D. | Cl-、CO32-、K+、Na+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 0℃ | 30℃ | 60℃ | 90℃ | |
| 甲 | 13.3克 | 45.8克 | 110克 | 202克 |
| 乙 | 35.5克 | 36.0克 | 37.1克 | 38.1克 |
| 丙 | 0.18克 | 0.16克 | 0.12克 | 0.08克 |
| A. | 降低温度可使丙的不饱和溶液变为饱和溶液 | |
| B. | 甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙 | |
| C. | 0℃时,三种物质的饱和溶液溶质质量分数甲>乙>丙 | |
| D. | 使乙物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
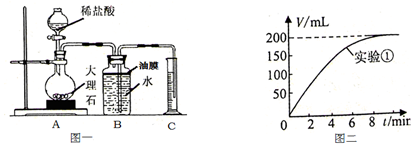
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食盐溶液、蔗糖溶液是$\stackrel{推断}{→}$无色的无色的液体都是溶液 | |
| B. | 在室温下的硝酸钾饱和溶液$\stackrel{推测}{→}$此时该溶液不能再溶解其它任何物质了 | |
| C. | 粉末状食盐比粗的颗粒状食盐溶解快$\stackrel{解释}{→}$由于物质的溶解性与颗粒大小有关 | |
| D. | 氢氧化钠溶于水时温度会升高$\stackrel{归纳}{→}$有些物质溶解时会放热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com