
要将80 溶质质量分数为10%的食盐溶液变成20%的溶液,可采用的方法为( )
A、将溶剂蒸发掉原溶剂质量的一半
B、将溶剂蒸发掉原溶液质量的一半
C、将溶质质量增加1倍
D、将溶质质量增加2倍![]()
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 相关的质量 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 所加入稀盐酸的质量(g) | 50 | 50 | 50 | 50 | 50 |
| 烧杯中剩余的质量(g) | 72.8 | 120.6 | 168.4 | 216.2 | 266.2 |
| 100 |
| x |
| 44 |
| 8.8g |
| 100 |
| x |
| 44 |
| 8.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
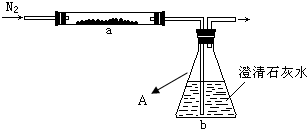
 2M+CO2↑和______(请再举一例,用化学方程式表示),请补全题干中的实验步骤______.
2M+CO2↑和______(请再举一例,用化学方程式表示),请补全题干中的实验步骤______. 2M+CO2↑,则1.8g的MO与0.12g的C充分反应,①生成的二氧化碳至少需要溶质质量发生为0.1%的澄清石灰水多少g才能完全吸收,转化为碳酸钙?(MO的相对分子质量为80)(本题2分,写出计算过程)
2M+CO2↑,则1.8g的MO与0.12g的C充分反应,①生成的二氧化碳至少需要溶质质量发生为0.1%的澄清石灰水多少g才能完全吸收,转化为碳酸钙?(MO的相对分子质量为80)(本题2分,写出计算过程)查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
下表是NaCl和KCl的溶解度数据,请回答下列问题。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
(1)40℃时,氯化钠的溶解度是 g。
(2)将80℃时, 同质量的NaCl和KCl的饱和溶液,分别冷却到0℃,析出晶体最多的是_ (填“NaCl”或“KCl”)溶液。
(3)20℃时,向两只分别盛有35 g NaCl和KCl固体的烧杯中,各加入100g水,充分溶解后,能形成饱和溶液的物质是 ,其溶液的溶质质量分数是______(精确到0.1%)。
(4)温度不变的情况下,若要将接近饱和的KCl溶液变成饱和溶液,可采用的方法是_______________。(写一种)
 Ⅱ.(6分)阅读下列三段材料,回答问题:
Ⅱ.(6分)阅读下列三段材料,回答问题:
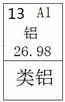
材料一:l869年,俄国化学家门捷列夫对已发现的元素进行研究,制作了元素周期表(右表是其片断),并在他的元素周期表中留下了许多空位代表尚未发现的新元素,其中就预言了“类铝”这种新元素。
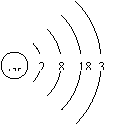 材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料三:l876年,布瓦博德朗将金属镓提纯后测得镓的密度为
5.94g·cm-3,从而验证了元素周期表的正确性。随后科学家根据元素
周期表的空位,按图索骥,发现了许多新元素。目前金属镓广泛用于
制造半导体材料。镓的原子结构示意图如右图所示。
(1)镓元素的质子数为__________,其氯化物的化学式为_____________。
(2)请根据上述材料,小结金属镓的有关知识:
① 物理性质:镓是银白色金属,密度为5.94g·cm -3
-3
② 化学性质(请用化学方程式表示):_____________________________________;
③ 用途:____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
下表是NaCl和KCl的溶解度数据,请回答下列问题。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
(1)40℃时,氯化钠的溶解度是 g。
(2)将80℃时, 同质量的NaCl和KCl的饱和溶液,分别冷却到0℃,析出晶体最多的是_ (填“NaCl”或“KCl”)溶液。
(3)20℃时,向两只分别盛有35 g NaCl和KCl固体的烧杯中,各加入100g水,充分溶解后,能形成饱和溶液的物质是 ,其溶液的溶质质量分数是______(精确到0.1%)。
(4)温度不变的情况下,若要将接近饱和的KCl溶液变成饱和溶液,可采用的方法是_____
___________。(写一种)
 Ⅱ.(6分)阅读下列三段材料,回答问题:
Ⅱ.(6分)阅读下列三段材料,回答问题:
材料一:l869年,俄国化学家门捷列夫对已发现的元素进行研究,制作了元素周期表(右表是其片断),并在他的元素周期表中留下了许多空位代表尚未发现的新元素,其中就预言了“类铝”这种新元素。
 材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料三:l876年,布瓦博德朗将金属镓提纯后测得镓的密度为
5.94g·cm-3,从而验证了元素周期表的正确性。随后科学家根据元素
周期表的空位,按图索骥,发现了许多新元素。目前金属镓广泛用于
制造半导体材料。镓的原子结构示意图如右图所示。
(1)镓元素的质子数为__________,其氯化物的化学式为_____________。
(2)请根据上述材料,小结金属镓的有关知识:
① 物理性质:镓是银白色金属,密度为5.94g·c m-3
m-3
② 化学性质(请用化学方程式表示):_____________________________________;
③ 用途:____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com