
| A. | 将Zn、Cu分别加入到FeSO4溶液中 | |
| B. | 把Zn分别加入到CuSO4溶液、FeSO4溶液中 | |
| C. | 把Zn、Cu分别加入到ZnSO4溶液中 | |
| D. | 把Cu分别加入到FeSO4溶液、ZnSO4溶液中 |
分析 在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;氢前的金属能与酸反应生成氢气,且金属的活动性越强产生气泡的速率越快,但要注意控制变量的运用.
解答 解:A、在金属活动性顺序中,由于金属锌在铁前,铜在铁后,因此锌可以和硫酸亚铁溶液反应,在锌的表面有一层银白色的物质生成,而铜不能和硫酸亚铁溶液反应,从而证明了三种金属的活动性顺序:锌>铁>铜,故A正确;
B、由于在金属活动性顺序中,铁、铜在锌的后面,因此铜不能和硫酸锌溶液反应,铁也不和硫酸锌溶液反应,只能证明锌的活动性比铜、铁强,但无法比较铁与铜的活动性顺序,故B错误;
C、由于在金属活动性顺序中,铜在锌的后面,因此铜不能和硫酸锌溶液反应,锌也不和硫酸锌溶液反应,只能证明锌的活动性比铜强,但无法比较铁与锌、铜的活动性顺序,故C错误;
D、由于在金属活动性顺序中,铜在锌和铁的后面,因此铜不能和硫酸亚铁溶液反应,也不和硫酸锌溶液反应,只能证明铁、锌的活动性比铜强,但无法比较铁与锌的活动性顺序,故D错误;
故选:A
点评 本题考查了金属活动性顺序的应用,要求要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.能够很好的考查学生对金属活动性顺序的应用和理解,培养学生的应用能力和理解能力.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题
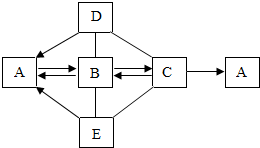 A-E是初中化学常见的五种物质,D、E是氧化物.常温下,B是气体,D是黑色固体,E是红棕色固体. A、B、C含氢元素,胃液中含C.短线“-”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:
A-E是初中化学常见的五种物质,D、E是氧化物.常温下,B是气体,D是黑色固体,E是红棕色固体. A、B、C含氢元素,胃液中含C.短线“-”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 绿原酸属于混合物 | |
| B. | 绿原酸的相对分子质量为354 | |
| C. | 绿原酸中氧元素的质量分数最高 | |
| D. | 绿原酸中碳、氢元素的质量比为16:18 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +4 | B. | +5 | C. | +6 | D. | +7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
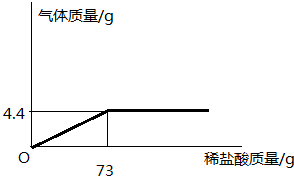 有NaCl和Na2CO3组成的混合物13.5g完全溶于63.9g水中,向得到的溶液中加入稀盐酸.如图:
有NaCl和Na2CO3组成的混合物13.5g完全溶于63.9g水中,向得到的溶液中加入稀盐酸.如图:查看答案和解析>>
科目:初中化学 来源: 题型:解答题



查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com