
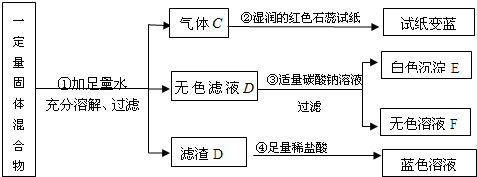
 ŹŖ·ØŅ±Ķ³§ÅŷŵķĻĖ®ÖŠŗ¬ÓŠĮņĖįŗĶĮņĖįĶĮ½ÖÖĪŪČ¾Īļ£¬ĪŖ²ā¶ØøĆ·ĻĖ®ÖŠø÷ĪŪČ¾ĪļµÄŗ¬Į棬»·±£Š”×éµÄĶ¬Ń§½ųŠŠĮĖŅŌĻĀŹµŃé£®Č”·ĻĖ®500g£¬ĻņĘäÖŠ¼ÓČėČÜÖŹÖŹĮæ·ÖŹżĪŖ20%µÄĒāŃõ»ÆÄĘČÜŅŗ£®²āµĆ³ĮµķÖŹĮæÓėĖł¼ÓČėµÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼£®øł¾ŻĖłµĆŹż¾Ż¼ĘĖć£ŗ
ŹŖ·ØŅ±Ķ³§ÅŷŵķĻĖ®ÖŠŗ¬ÓŠĮņĖįŗĶĮņĖįĶĮ½ÖÖĪŪČ¾Īļ£¬ĪŖ²ā¶ØøĆ·ĻĖ®ÖŠø÷ĪŪČ¾ĪļµÄŗ¬Į棬»·±£Š”×éµÄĶ¬Ń§½ųŠŠĮĖŅŌĻĀŹµŃé£®Č”·ĻĖ®500g£¬ĻņĘäÖŠ¼ÓČėČÜÖŹÖŹĮæ·ÖŹżĪŖ20%µÄĒāŃõ»ÆÄĘČÜŅŗ£®²āµĆ³ĮµķÖŹĮæÓėĖł¼ÓČėµÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼£®øł¾ŻĖłµĆŹż¾Ż¼ĘĖć£ŗ·ÖĪö ¢Łøł¾Żn=$\frac{m}{M}$½ųŠŠ¼ĘĖć£»
¢Śøł¾ŻĒāŃõ»ÆÄĘÓėĮņĖįĶ·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬ĄūÓĆÉś³É³ĮµķµÄĪļÖŹµÄĮææɼĘĖć³ö·ĻĖ®ÖŠĮņĖįĶµÄĪļÖŹµÄĮ棬»»ĖćĮņĖįĶÖŹĮ棻
¢ŪÓÉĶ¼Ź¾æÉÖŖÓėĮņĖį·“Ó¦µÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæĪŖ40g£¬æÉŅŌ»»Ėć³ö·“Ó¦ĖłĻūŗÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮ棬øł¾ŻĮņĖįÓėĒāŃõ»ÆÄĘ·“Ó¦µÄ·½³ĢŹ½¼ĘĖć³ö·ĻĖ®ÖŠĮņĖįµÄĪļÖŹµÄĮ森
½ā“š ½ā£ŗ
¢ŁµĆµ½ĒāŃõ»ÆĶ³ĮµķµÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{19.6g}{98g/mol}$=0.2mol£»
¢ŚÉč·ĻĖ®ÖŠĮņĖįĶµÄĪļÖŹµÄĮæĪŖx£¬ĻūŗĵÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĪŖy£®
CuSO4+2NaOH=Cu£ØOH£©2”ż+Na2SO4
1 1
x 0.2mol
$\frac{1}{x}$=$\frac{1}{0.2mol}$
x=0.2mol£»
øĆ·ĻĖ®ÖŠĮņĖįĶµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ$\frac{160g/mol”Į0.2mol}{500g}$”Į100%=6.4%
¢ŪÓėĮņĖį·“Ó¦µÄĒāŃõ»ÆÄʵÄÖŹĮæĪŖ40g”Į20%=8g
ÓėĮņĖį·“Ó¦µÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{8g}{40g/mol}$=0.2mol
ÉčøĆ·ĻĖ®ÖŠĮņĖįµÄĪļÖŹµÄĮæŹĒy
H2SO4+2NaOH=Na2SO4+2H2O
1 2
y 0.2mol
$\frac{1}{y}$=$\frac{2}{0.2mol}$
y=0.1mol
“š£ŗ¢Ł0.2£»¢Ś6.4%
¢Ū0.1mol
µćĘĄ ¶Ō·“Ó¦µÄĶ¼ĻóÖŠĒśĻß½ųŠŠ·ÖĪö£¬øĆĒśĻßµÄĘšµć±ķŹ¾ĮņĖį±»ĶźČ«·“Ó¦”¢ÕŪµć±ķŹ¾ĮņĖįĶÓėĒāŃõ»ÆÄĘĒ”ŗĆĶźČ«·“Ó¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
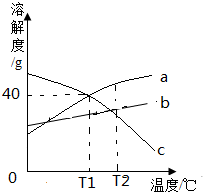 a”¢b”¢cČżÖÖĪļÖŹµÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
a”¢b”¢cČżÖÖĪļÖŹµÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | aČÜŅŗÖŠŗ¬ÓŠÉŁĮæµÄb£¬ČōŅŖĢį“æa£¬ŌņæɲŲÉÓĆÕō·¢½į¾§µÄ·½·Ø | |
| B£® | T2”ꏱµÄµČÖŹĮæµÄČżÖÖĪļÖŹµÄ±„ŗĶČÜŅŗĶ¬Ź±½µĪĀµ½T1”ę£¬ĖłµĆČżÖÖČÜŅŗµÄÖŹĮæ·ÖŹżĪŖa=c£¾b | |
| C£® | ŌŚT1”ꏱ£¬25gµÄaČÜÓŚ40gĖ®ÖŠ£¬ĖłµĆČÜŅŗµÄÖŹĮæĪŖ56g | |
| D£® | T2”ꏱȿÖÖĪļÖŹČÜÖŹµÄÖŹĮæ·ÖŹżĪŖa£¾b£¾c |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó³ŹµēÖŠŠŌ | |
| B£® | Ō×ÓŗĖ¶¼ŹĒÓÉÖŹ×ÓŗĶÖŠ×Ó¹¹³É | |
| C£® | Ō×ÓÓÉŌ×ÓŗĖÓėŗĖĶāµē×Ó¹¹³É | |
| D£® | Ō×Óæɹ¹³É·Ö×Ó£¬ÓŠµÄŅ²æÉÖ±½Ó¹¹³ÉĪļÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
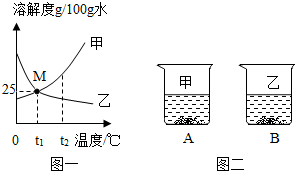 Ķ¼Ņ»ĪŖ¼×”¢ŅŅĮ½ÖÖĪļÖŹ£Ø²»“ų½į¾§Ė®£©µÄČܽā¶ČĒśĻßĶ¼£®
Ķ¼Ņ»ĪŖ¼×”¢ŅŅĮ½ÖÖĪļÖŹ£Ø²»“ų½į¾§Ė®£©µÄČܽā¶ČĒśĻßĶ¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  Ńõ»ÆøĘČÜŅŗ | B£® |  ÉÕ¼īČÜŅŗ | C£® |  µØ·ÆČÜŅŗ | D£® |  Ź³ŃĪČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 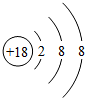 »ÆѧŠŌÖŹĪČ¶Ø | B£® | 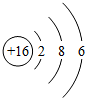 Ņ׊Ī³ÉŅõĄė×Ó | C£® | 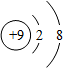 “ųÕżµēŗÉ | D£® | 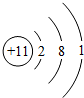 Ņ׏§µē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĮÖĘĘ·¾¾ĆÄĶÓĆ--ĀĮ±Č½Ļ²»»īĘĆ | |
| B£® | Ļū·ĄŌ±ÅēĖ®ĆšĖ®µÄŌĄķ--øō¾ųæÕĘų | |
| C£® | CaOæÉ×÷Ź³Ę·øÉŌļ¼Į--CaOÓŠŗÜĒæµÄĪüĖ®ŠŌ | |
| D£® | ĀĢÉ«Ö²Īļ¹āŗĻ×÷ÓĆĪüŹÕĢ«ŃōÄÜ--Ģ«ŃōÄÜ×Ŗ»ÆĪŖČČÄÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 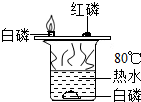 ŃéÖ¤æÉČ¼ĪļČ¼ÉÕµÄĢõ¼ž | |
| B£® | 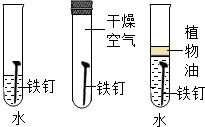 Ģ½¾æĢśÉśŠāµÄĢõ¼ž | |
| C£® | 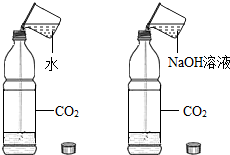 Ö¤Ć÷CO2ŗĶNaOH·“Ó¦ | |
| D£® | 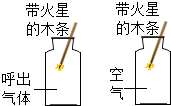 Ģ½¾æŗō³öĘųĢåŗĶæÕĘųÖŠŃõĘųŗ¬ĮæµÄ²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com