
| 0”ę | 20”ę | 40”ę | 60”ę | |
| NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
| NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
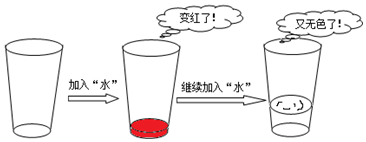
·ÖĪö £Ø1£©øł¾Ż±ķÖŠĀČ»ÆÄĘČܽā¶ČĖęĪĀ¶Č±ä»ÆµÄĒéæö»Ų“š£®
£Ø2£©øł¾Ż±ķÖŠĀČ»ÆÄĘČܽā¶ČĖęĪĀ¶Č±ä»ÆµÄĒéæö»Ų“š£®
£Ø3£©øł¾Ż±ķÖŠĢ¼ĖįĒāÄĘŌŚµĶĪĀĻĀČܽā¶ČŗÜŠ”£¬Ņ×½į¾§Īö³ö£¬ŠĪ³É³ĮµķĪļµÄĢŲµćŅŌ¼°ŃĪµÄĢŲµć»Ų“š£®
½ā“š ½ā£ŗ£Ø1£©“Ó±ķÖŠæÉŅŌ擳ö£¬ĪĀ¶Č¶ŌNaHCO3ŗĶNH4ClµÄČܽā¶ČµÄÓ°Ļģ¶¼±Č½Ļ“󣬶ŌNaClµÄČܽā¶ČÓ°Ļģ²»“ó£®
£Ø2£©Ėę×ÅĪĀ¶ČµÄÉżøߣ¬NH4ClµÄČܽā¶Č±ä“ó£¬ĒŅŹÜĪĀ¶Č±ä»ÆÓ°Ļģ“ó£¬æÉŅŌĶعżŌŚ½ĻøßĪĀ¶ČĻĀÅäÖĆNH4ClµÄ±„ŗĶČÜŅŗ£¬Č»ŗóŌŁ½µĪĀ½į¾§Īö³öNH4ClµÄ°ģ·Ø½«NH4Cl“ÓČÜŅŗÖŠ·ÖĄė³öĄ“£®
£Ø3£©NaCl+CO2+NH3+H2OØTNaHCO3”ż+NH4ClÕāøö·“Ó¦Äܹ»½ųŠŠ£¬ŹĒŅņĪŖNaHCO3ŌŚĖ®ÖŠµÄČܽā¶Č½ĻŠ”£¬æÉŅŌ½į¾§Īö³ö£¬Ļąµ±Éś³ÉĮĖ³Įµķ£¬·ūŗĻø“·Ö½ā·“Ó¦µÄ»ł±¾Ģõ¼ž£¬»Æѧ·½³ĢŹ½ĪŖ£ŗNaCl+CO2+NH3+H2OØTNaHCO3”ż+NH4Cl£®“æ¼īŹĒÓÉÄĘĄė×ÓŗĶĢ¼ĖįøłĄė×Ó¹¹³ÉµÄ£¬ŹōÓŚŃĪĄąĪļÖŹ£¬Ģ¼ĖįÄĘÄÜÓėĒāŃõ»ÆøĘ·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĒāŃõ»ÆÄĘ£¬»Æѧ·½³ĢŹ½ĪŖ£ŗCa£ØOH£©2+Na2CO3ØTCaCO3”ż+2NaOH£®
¹Ź“š°øĪŖ£ŗ£Ø1£©NaCl£»
£Ø2£©½ĻµĶ£»
£Ø3£©NaCl+CO2+NH3+H2OØTNaHCO3”ż+NH4Cl£»ŃĪ£»Ca£ØOH£©2+Na2CO3ØTCaCO3”ż+2NaOH£®
µćĘĄ »ÆѧĄ“Ō“ÓŚÉś²ś”¢Éś»ī£¬ÓÖ·žĪńÓŚÉś²ś”¢Éś»ī£¬°±¼ī¹¤ŅµŹĒ³õÖŠ»ÆѧÖŲŅŖµÄÓ¦ÓĆÖ®Ņ»£¬ŹĒæ¼²éÖŲµć£¬³£Éę¼°»Æѧ·½³ĢŹ½µÄŹéŠ“£¬¶žŃõ»ÆĢ¼ŗĶ°±ĘųĶØČėµÄĖ³Šņ¼°ŌŅņ£¬·“Ó¦Ź±Īö³öĢ¼ĖįĒāÄʵÄŌŅņÓėĪļÖŹČܽā¶ČµÄ¹ŲĻµµČÖŲµćÄŚČŻ£®


 Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø
Č«ÄÜĮ·æ¼¾ķĻµĮŠ“š°ø Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
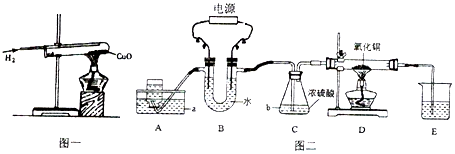
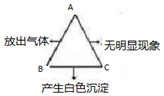 ČēĶ¼ĖłŹ¾µÄA”¢B”¢CČżÖÖČÜŅŗĮ½Į½»ģŗĻ£¬·¢ÉśĮĖ»Æѧ·“Ó¦Ķ¬Ź±²śÉśµÄŹµŃéĻÖĻó£¬ĘäÖŠAŹĒ³õÖŠ»Æѧ³£¼ūµÄĖį£¬ĒėŠ“³ö·ūŗĻŹµŃéĻÖĻóµÄŅ»×éĪļÖŹµÄ»ÆѧŹ½ŗĶŅ»øö»Æѧ·½³ĢŹ½£®
ČēĶ¼ĖłŹ¾µÄA”¢B”¢CČżÖÖČÜŅŗĮ½Į½»ģŗĻ£¬·¢ÉśĮĖ»Æѧ·“Ó¦Ķ¬Ź±²śÉśµÄŹµŃéĻÖĻó£¬ĘäÖŠAŹĒ³õÖŠ»Æѧ³£¼ūµÄĖį£¬ĒėŠ“³ö·ūŗĻŹµŃéĻÖĻóµÄŅ»×éĪļÖŹµÄ»ÆѧŹ½ŗĶŅ»øö»Æѧ·½³ĢŹ½£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź³ŃĪŗĶĖ®ŠĪ³ÉµÄČÜŅŗ | B£® | Ź³ŃĪĖ®ŗĶÄąÉ³ŠĪ³ÉµÄŠü×ĒŅŗ | ||
| C£® | Ź³ÓĶŗĶĖ®ŠĪ³ÉµÄČé×ĒŅŗ | D£® | ¾Ę¾«ŗĶĖ®µÄ»ģŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé | ŹŌ¹Ü1 | ŹŌ¹Ü2 | ŹŌ¹Ü3 |
| ŹµŃé²Ł×÷ |  |  | 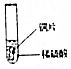 |
| ŹµŃéĻÖĻó | ½šŹōX±ķĆę²śÉśĘųÅŻ»ŗĀż | ½šŹōŠæ±ķĆę²śÉśĘųÅŻ½Ļæģ | ²»²śÉśĘųÅŻ |
| ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| ȔɣĮæµÄĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬ŌŚĀĖŅŗÖŠ¼ÓČė Ļ”ŃĪĖį£® | ²śÉś°×É«³Įµķ | ²ĀĻė¢Ū³ÉĮ¢ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
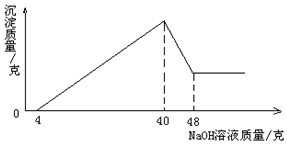 ×¼Č·³ĘČ”5æĖĀĮĶĮæó£Øŗ¬Al2O3£¬Fe2O3£¬SiO2£©ŃłĘ·£¬·ÅČėŹ¢ÓŠ50æĖÄ³ÖŹĮæ·ÖŹżµÄĮņĖįČÜŅŗµÄÉÕ±ÖŠ£¬³ä·Ö·“Ó¦ŗó¹żĀĖ£¬ŌŁĻņĀĖŅŗÖŠ¼ÓČė20%µÄĒāŃõ»ÆÄĘČÜŅŗ£¬²śÉś³ĮµķµÄÖŹĮæÓėĖł¼ÓČėµÄĒāŃõ»ÆÄĘČÜŅŗÖŹĮæµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®
×¼Č·³ĘČ”5æĖĀĮĶĮæó£Øŗ¬Al2O3£¬Fe2O3£¬SiO2£©ŃłĘ·£¬·ÅČėŹ¢ÓŠ50æĖÄ³ÖŹĮæ·ÖŹżµÄĮņĖįČÜŅŗµÄÉÕ±ÖŠ£¬³ä·Ö·“Ó¦ŗó¹żĀĖ£¬ŌŁĻņĀĖŅŗÖŠ¼ÓČė20%µÄĒāŃõ»ÆÄĘČÜŅŗ£¬²śÉś³ĮµķµÄÖŹĮæÓėĖł¼ÓČėµÄĒāŃõ»ÆÄĘČÜŅŗÖŹĮæµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
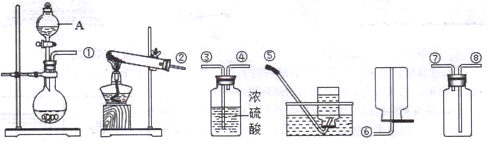
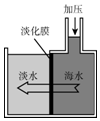 ŗ£Ė®µ»ÆæɲÉÓĆĤ·ÖĄė¼¼Źõ£®ČēĶ¼ĖłŹ¾£¬¶Ōµ»ÆĤÓŅ²ąµÄŗ£Ė®¼ÓŃ¹£¬Ė®·Ö×ÓæÉĶø¹żµ»ÆĤ½ųČė×ó²ąµĖ®³Ų£¬¶ųŗ£Ė®ÖŠø÷ÖÖČÜÖŹ²»ÄÜĶعżµ»ÆĤ£¬“Ó¶ųµĆµ½µĖ®£®¶Ō¼ÓŃ¹ŗóÓŅ²ąŗ£Ė®³É·Ö±ä»Æ·ÖĪöÕżČ·µÄŹĒ£Ø””””£©
ŗ£Ė®µ»ÆæɲÉÓĆĤ·ÖĄė¼¼Źõ£®ČēĶ¼ĖłŹ¾£¬¶Ōµ»ÆĤÓŅ²ąµÄŗ£Ė®¼ÓŃ¹£¬Ė®·Ö×ÓæÉĶø¹żµ»ÆĤ½ųČė×ó²ąµĖ®³Ų£¬¶ųŗ£Ė®ÖŠø÷ÖÖČÜÖŹ²»ÄÜĶعżµ»ÆĤ£¬“Ó¶ųµĆµ½µĖ®£®¶Ō¼ÓŃ¹ŗóÓŅ²ąŗ£Ė®³É·Ö±ä»Æ·ÖĪöÕżČ·µÄŹĒ£Ø””””£©| A£® | ČÜÖŹÖŹĮæŌö¼Ó | B£® | ČÜŅŗÖŹĮæŌö¼Ó | ||
| C£® | ČÜÖŹµÄÖŹĮæ²»±ä | D£® | ČÜÖŹÖŹĮæ·ÖŹż¼õÉŁ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com