
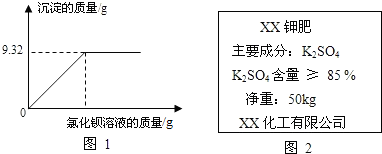
分析 从图象中看出生成的沉淀的质量是9.32g,根据硫酸钾和氢氧化钡会生成硫酸钡沉淀,利用化学方程式计算出硫酸钾的质量,再算出质量分数与标准比较从而判断是否符合包装说明;
解答 解:由图可知,生成的BaSO4质量为9.32g,设8.0g钾肥样品中含有硫酸钾的质量为x,
K2SO4+BaCl2═BaSO4↓+2KCl
174 233
x 9.32g
$\frac{174}{x}=\frac{233}{9.32g}$
解得x=6.96g
则样品中硫酸钾的质量分数为:$\frac{6.96g}{8g}$×100%=87%
由于87%>85%,该钾肥中硫酸钾的质量分数符合产品包装说明.
答案:该钾肥中硫酸钾的质量分数符合产品包装说明.
点评 该题属于标签图象型计算题,主要考查读图能力,注意解题的格式要规范.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量碳酸氢钠于试管中,加适量水溶解, 再滴入几滴无色酚酞试液 | 无色酚酞试液变红色 | 猜想一正确 |

| 实验操作 | 实验现象 | 实验结论 |
| 实验一:取少量反应后的白色固体溶于水, 滴几滴无色酚酞试液 | 溶液变成红色 | 白色固体一定是NaOH |
| 实验二:取少量反应后的白色固体溶于水, 加入过量氯化钙溶液 | 产生白色沉淀 | 白色固体含有Na2CO3 |
| 实验三:取实验二所得的上层清液于试管中, 滴加几滴无色酚酞试液 | 无色酚酞试液不变色 | 白色固体是Na2CO3,而不是NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
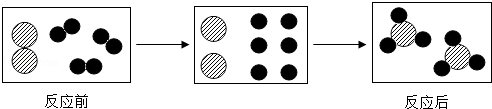
| A. | 反应前后元素种类发生改变 | |
| B. | 该反应的基本类型是化合反应 | |
| C. | 反应前后分子种类不发生改变 | |
| D. | 参加反应的两种分子的个数比是1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com