
| 20℃时,一些物质的溶解度 | ||
| OH- | CO32- | |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
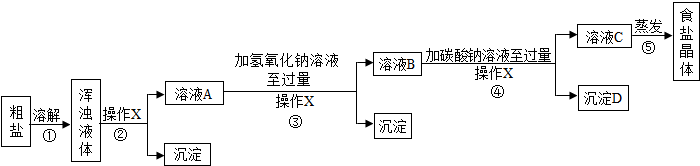
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
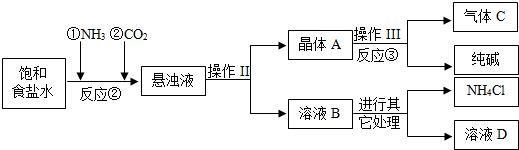
| ||
| ||
| 10.6g |
| 10.8g |
| ||
| ||


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:初中化学 来源: 题型:
| A、称量时,将固体NaCl放在天平左盘称量纸上 |
| B、蒸发操作中,玻璃棒的主要作用是加快蒸发 |
| C、主要操作步骤为:计算、称量、量取、溶解等 |
| D、量取时,视线与量筒内凹液面的最低点保持水平 |
查看答案和解析>>
科目:初中化学 来源: 题型:
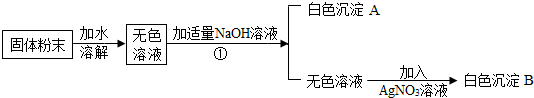
查看答案和解析>>
科目:初中化学 来源: 题型:
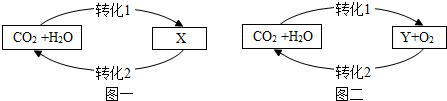
查看答案和解析>>
科目:初中化学 来源: 题型:
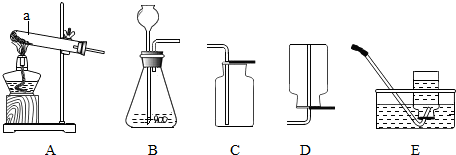
查看答案和解析>>
科目:初中化学 来源: 题型:
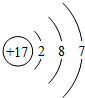 如图所示是某元素的原子结构示意图.该原子在化学反应中容易
如图所示是某元素的原子结构示意图.该原子在化学反应中容易查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具.如图是一种照明用台灯.
青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具.如图是一种照明用台灯.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com