
分析 铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜;由题意,将足量的铁片投入到80.0g硫酸铜溶液中,溶液的质量变为79.2g,由质量守恒定律,则金属的质量应增加80.0g-79.2g=0.8g,据此结合固体差量进行分析解答.
解答 解:设参加反应的铁片的质量为x,硫酸铜的质量为y,
Fe+CuSO4═FeSO4+Cu 固体差量
56 160 64 64-56=8
x y 0.8g
(1)$\frac{56}{8}=\frac{x}{0.8g}$ x=5.6g
(2)$\frac{160}{8}=\frac{y}{0.8g}$ y=16g
原硫酸铜溶液中溶质的质量分数为$\frac{16g}{80.0g}$×100%=20%.
答:(1)参加反应的铁片的质量为5.6g;(2)原硫酸铜溶液中溶质的质量分数为20%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,利用固体差量法是正确解答本题的关键.


科目:初中化学 来源: 题型:多选题
| A | B | C | D |
| 铁加入稀盐酸 | 向一定量的稀盐酸中加入铁粉 | 向两份体积和质量分数相同的盐酸中分别加入足量的铁粉和镁粉 | 向等质量的金属镁和铝中分别滴加足量且溶质质量分数相等的稀硫酸 |
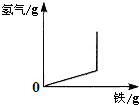 | 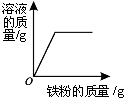 | 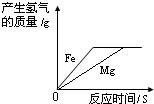 | 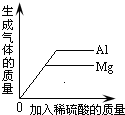 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯原子得到1个电子形成带负电荷的氯离子 | |
| B. | 原子是由质子和中子构成的 | |
| C. | 分子的质量总比原子的质量大 | |
| D. | 保持水的化学性质的粒子是氢原子和氧原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加药品 | B. | 调节平衡螺母 | C. | 减少药品 | D. | 加砝码 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | A | B | C | D |
| 反应前的质量/g | 4 | 6 | 111 | 4 |
| 反应后的质量/g | 待测 | 15 | 0 | 84 |
| A. | 容器中发生的化学变化一定属于置换反应 | |
| B. | 容器中发生的化学变化属于化合反应 | |
| C. | 参加反应的物质和生成的物质其质量比为111:22:9:80 | |
| D. | 反应后密闭容器中A的待测质量为22g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是A、B、C三种物质的溶解度曲线图,看图后回答下列问题:
如图是A、B、C三种物质的溶解度曲线图,看图后回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
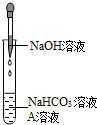 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com