
| A. | 铝-铁合金 | B. | 镁-锌合金 | C. | 锌-铁合金 | D. | 铁-铜合金 |
分析 根据一定量金属与足量酸完全反应时,产生氢气质量=$\frac{金属化合价}{金属相对原子质量}$×金属质量,可计算产生0.2g氢气消耗铁的质量恰好为5.6g,所以其余两种杂质金属产生同样多氢气时消耗金属质量一种大于5.6g,一种小于5.6g.
解答 解:得到0.2g氢气需要消耗金属铁的质量m,$\frac{2}{56}$×m=0.2g,则m=5.6g,所以铁样品中另两种金属为:产生0.2g氢气,需要金属的质量一种大于5.6g,另一种小于5.6g;
根据一定量金属与足量酸完全反应时,产生氢气质量=$\frac{金属化合价}{金属相对原子质量}$×金属质量,可计算得知,产生0.2g氢气,消耗铝、镁的质量为1.8克、2.4克,都小于5.6g而消耗锌的质量为6.5克,大于5.6g,铜不能与酸反应产生氢气,说明消耗铜的质量大于5.6g;因此可判断样品中的两种金属杂质为金属铝、镁中的一种和金属锌、铜中一种;
故选B.
点评 相同质量的金属镁、铝、锌、铁完成反应放出氢气的质量由大到小的顺序为铝>镁>铁>锌.


 互动英语系列答案
互动英语系列答案科目:初中化学 来源: 题型:选择题
| A. | 实验室制O2结束时,先熄灭酒精灯再把导管移出水面 | |
| B. | 在测量小石块密度的时候,先用量筒测石块的体积,再用天平测石块的质量 | |
| C. | 一氧化碳还原氧化铜实验结束时,先移去酒精灯,冷却后再取出通氢气的导管 | |
| D. | 稀释浓硫酸时,先在烧杯内倒入浓硫酸,再缓慢注入水,并不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
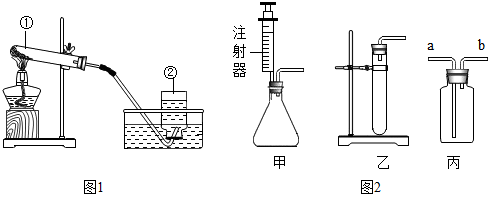
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①⑤⑥ | B. | ③⑤⑥ | C. | ②③⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | Fe在Ⅰ、Ⅱ两类反应中的产物不相同 | |
| B. | Ⅱ中Fe、Al氧化均能生成致密的氧化物薄膜,可阻止其进一步被氧化 | |
| C. | S、P、Mg在氧气中燃烧均会产生大量白烟 | |
| D. | Ⅰ类反应放出热量,Ⅱ类反应吸收热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com