
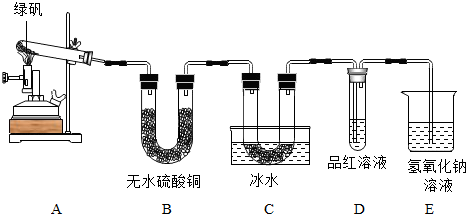
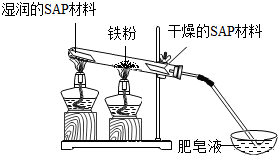
 已知Mg能在CO2中燃烧生成碳和一种白色固体物质,某化学兴趣小组用如图所示装置制备CO2并对Mg在CO2中燃烧生成的白色固体物质进行探究.
已知Mg能在CO2中燃烧生成碳和一种白色固体物质,某化学兴趣小组用如图所示装置制备CO2并对Mg在CO2中燃烧生成的白色固体物质进行探究.分析 (1)熟记常见仪器的名称;
(2)根据盐酸会发出的氯化氢气体能与碳酸氢钠溶液反应生成氯化钠、水和二氧化碳;浓硫酸具有吸水性;
(3)二氧化碳不能燃烧,不支持燃烧;
(4)根据质量守恒定律来分析;根据碳酸镁和氧化镁与盐酸反应的实验现象来分析.
解答 解:(1)仪器a的名称是长颈漏斗;故填:长颈漏斗;
(2)碳酸氢钠溶液能除去盐酸挥发出来的氯化氢气体,氯化氢气体溶于水后形成盐酸,盐酸与碳酸氢钠反应生成氯化钠、水和二氧化碳,浓硫酸具有吸水性,对二氧化碳气体起到了干燥的作用;故填:NaHCO3+HCl=NaCl+H2O+CO2↑;干燥;
(3)检验二氧化碳是否已充满集气瓶的方法是:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.故填:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.
(4)①化学反应前后元素的种类不变,而反应物中没有氢元素,所以猜想Ⅱ错误;故填:Ⅱ;反应物中没有氢元素;
②碳酸镁与盐酸反应生成氯化镁、二氧化碳和水,而氧化镁与盐酸反应生成氯化镁和水,此实验中没有气体生成,所以固体是氧化镁,猜想Ⅰ合理;镁在二氧化碳中燃烧生成氧化镁和碳;故填:Ⅰ;2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 熟记实验室制取二氧化碳的反应原理、实验步骤、装置示意图、注意事项以及物质的检验和除杂的知识,依据已有的知识进行解答,要求同学们在平时的学习中加强基础知识的储备,以便能够灵活应用.


 优学名师名题系列答案
优学名师名题系列答案科目:初中化学 来源: 题型:选择题
| A. | 对二甲苯属于有机高分子化合物 | |
| B. | 对二甲苯中碳元素的质量分数大于甲烷中碳元素的质量分数 | |
| C. | 对二甲苯是由8个碳原子和10个氢原子构成 | |
| D. | 对二甲苯中碳元素、氢元素的质量比为4:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热分解KClO3制氧气未加MnO2 | |
| B. | 电解水实验产生氧气的电极为负极 | |
| C. | 收集氧气时,用带火星的木条进行验满,这是利用了氧气的可燃性 | |
| D. | 铁丝在氧气中燃烧,火星四射,得到黑色固体物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com