
| ||
| ||
| 168 |
| x |
| 44 |
| 2.2g |
| 19g-8.4g |
| 19g |
| 23 |
| 84 |
| 46 |
| 106 |
| ||


 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、长期饮用硬水对人体的健康不利 |
| B、用洗洁精清洗餐具上的油污是乳化作用 |
| C、用氢氧化钠治疗胃酸过多 |
| D、空气中灼烧铜片后质量增加符合质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:
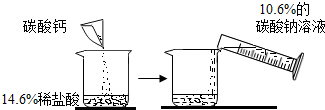
| 第一次 | 第二次 | |
| 14.6%的稀盐酸的质量 | m | m |
| 加入碳酸钙的质量 | 10g | 20g |
| 加入10.6%的碳酸钠溶液的质量 | 100g | 200g |
| 加入碳酸钠溶液后,实验现象 | 只有气泡 | 只有白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
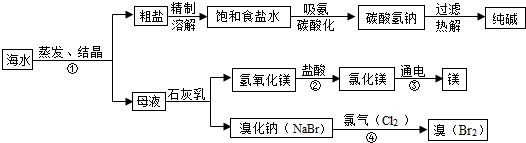
| 溶解物质 | 主要气体 | O2、CO2、H2S |
| 主要离子 | Cl-、CO32-、Na+ | |
| 生物生成物 | NH4+、HPO42-、Fe3+ | |
| 微量元素 | Br、I、F、Cu | |
| 悬浮物质 | 细菌、藻类、泥沙.黏土及其他不溶物 | |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com