
��ͼ��A��B��C�������ʵ��ܽ�����ߡ����������������

A. t1��ʱ���������ʵ��ܽ�ȴ�С˳��ΪA<B<C
B. t2��ʱ��A��B�������ʵ��ܽ�����
C. t3��ʱB�ı�����Һ���µ�t1�棬��ɲ�������Һ
D. ��Ҫ�������N���A��Һת��ΪM���A��Һ�����Բ�ȡ���������ܼ��ķ���
C ��������A�������������ʵ��ܽ�����߿�֪����t1��ʱ���������ʵ��ܽ�ȴ�С��ϵ��C��B��A����A��ȷ�� B��������t2��ʱ��A��B�����ʵ��ܽ�����߽���һ�㣬˵�������ʵ��ܽ����ȣ���B��ȷ�� C������B���ܽ�����¶ȵĽ��Ͷ���С����˸�B�ı�����Һ����ʱ��������Һ�оͻ��о�������������Һ��Ϊ������Һ����C���� D������N�����ܽ�������·�����������A�IJ�������Һ����...
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ���Ϻ���������2018�������ģ��ѧ�Ծ�word�溬�� ���ͣ���ѡ��
������ͭ�������������������Ļ����Һ�л���������������Ϊ m ��п�ۣ���Һ�����������������μӷ�Ӧ ��п��������ϵ��ͼ��ʾ��˵���������

A. bc �κ��еĽ����� Ag �� Cu
B. cd ����Һ������������
C. ��Ӧ��������Һ���������ϼ�С������п����������������
D. �� bc �κ� cd ����������������ȣ���μӷ�Ӧ��п������ m2-m1< m3-m2
C �������������˳�����K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au���ڽ����˳����У�������ǰ�ߵĽ����ܺ��ᷢ���û���Ӧ�����κ�������������λ��Խ��ǰ�������Ļ��Խǿ��λ�ÿ�ǰ�Ľ����ܽ�λ�����Ľ�������������Һ���û�����������п������������Ӧ������������п��a-b����Ȼ��������ͭ��Ӧ����ͭ������п��b-c������������������Ӧ������������п��...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����2018����꼶��ѧ�����п��Ի�ѧ�Ծ� ���ͣ�������
Ϊ�˲ⶨij������ˮ����������������ʵ����̺��й�ʵ��������ͼ��ʾ��

���㣺
��1����Ӧ�������Ȼ�����������_____g��
��2����������ˮ���������������Ƕ���_______������������ȷ��0.1%��
2.87g�� 0.9% ����������1���������غ㶨�ɿ�֪��Ӧǰ�����ʵ����������䣬��Ӧ�������Ȼ�����������130g+30g-157.13g= 2.87g����2�����������ˮ����������Ϊx NaCl +AgNO3 == AgCl��+ NaNO3 58.5 143.5 X 2.87g x=1.17g ������ˮ���������������� =0.9% �𣺸�������ˮ��������...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����2018����꼶��ѧ�����п��Ի�ѧ�Ծ� ���ͣ���ѡ��
�������ʵĻ�ѧ��������������Ӧ������ǣ�������
A. ������ˮ�� B. �������Ʃ�����ʯ�ҡ���ʯ��
C. ̼�����Ʃ���С�մ� D. �������Ʃ����ռ���������
D ��������A. ���׳�ˮ������ȷ�� B. ���������׳���ʯ�ҡ���ʯ�ң���ȷ��C. ̼�������׳�С�մ���ȷ�� D. ���������׳��ռ�ռ�����ƣ�̼�����׳ƴ���մ���ѡD���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������������2018����꼶��ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
�����д����л�ѧ��������ѧ�Ļ�ѧ֪ʶ��ա�
(1)����ȷ�Ļ�ѧ�������
����Ȼ����Ҫ�ɷּ���___________�ڵ������������ļ�__________ �۷��ͷ۵���Ҫ�ɷ�С�մ�__________ �ܲ�ͬ�ļ�������ƻ�ѧ������������Һ�ж�������ͬ��________
(2)�ҹ������������Ӳ�Ҵ�1999�꿪ʼ���У�һԪ��Ϊ��о����(Ni)����DZ�Ϊͭп�Ͻ�һ�DZ�Ϊþ���Ͻ�
����������Ӳ���õ��IJ��϶���_______(��ϳɲ��ϡ��������ϡ�)��ѡ������Ӳ�ҵIJ��ϲ���Ҫ���ǵ�������_________ (�����)��
A�������ĵ����� B����������ʴ�� C��������Ӳ��
�� ����Ӳ�����漰��Fe��Cu��Al��Ni(��)����֪���ܹ��������·�Ӧ
Ni+H2SO4�TH2��+NiSO4 Fe+NiCl2�TNi+FeCl2
��������Ӧ������___________��Ӧ (�ѧ������Ӧ����) �����ֽ����Ļ����ǿ������˳��Ϊ______________________(��Ԫ�ط��ű�ʾ)
CH4 Ca(OH)2 NaHCO3 OH- �������� A �û� Al��Fe��Ni ��Cu �����������⿼���˻�ѧʽ����д���������������ʼ���;���������˳����Ӧ�ã��������ϼ���Ӧ�ã���Ӧ���͵��ж��ȡ� (1) ����Ȼ����Ҫ�ɷּ��黯ѧʽΪCH4���ڵ������������ļ����������ƣ���ѧʽ��Ca(OH)2�� �۷��ͷ۵���Ҫ�ɷ�С�մ���̼�����ƣ���ѧʽ��NaHCO3 ���ܲ�ͬ�ļ�������ƻ�...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������������2018����꼶��ѧ�����п��Ի�ѧ�Ծ� ���ͣ���ѡ��
�ڴ����ᴿ��ʵ���У�����˵���������
A. �ܽ�����в������������ǽ��裬�Լӿ��Ȼ��Ƶ��ܽ��ٶ�
B. ���������е���Һȫ������ʱֹͣ����
C. �����������������������ʯ������
D. ʵ����������õ����Ȼ��ƹ��廹�ǻ����
B ��������A���ܽ�����в������������ǽ��裬Ŀ���Ǽӿ��Ȼ��Ƶ��ܽ��ٶȣ���ȷ��B��������Һʱ�����������г��ֽ϶����Ĺ���ʱ��Ӧֹͣ���ȣ��������Ƚ�ʣ��Һ�����ɣ�����C����������������Ӧ�����������ʯ�����ϣ��Է�ֹ�̻�ʵ��̨����ȷ��D�������ᴿֻ�dz�ȥ�˲��������ʣ�������һЩ�����Ե����ʣ����Ȼ�þ�ȣ���ʵ����������õ����Ȼ��ƹ��廹�ǻ�����ȷ����ѡB���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������2018����꼶��һ��ģ�⿼�Ի�ѧ�Ծ� ���ͣ���ѧ̽����
ij��ѧ��ȤС����һ�λ��������:��һ������ĺ�ɫ��ĩ��ɽ���̽����������벢�ش��й����⡣
����ʦ���ѡ�:����Cu��Fe2O3��Fe(OH)3���ֹ����е�һ�ֻ�������ɡ�
���������:����ɫ��ĩ���ܵ������: ��ֻ��Cu����ֻ��Fe2O3����ֻ��Fe(OH)3������Fe2O3��Fe(OH)3�Ļ�������Cu��Fe2O3�Ļ�������Cu��Fe(OH)3�Ļ���
�����ϻ�Ϥ��:
��1�������������ȷֽ�Ϊ��������ˮ����2����ɫ��ˮ����ͭ��ˮ������
��3�����������Ժ�ϡ���ᷴӦ�����Ȼ�����ˮ��
��4��ͭ�ڻ�ɫ�Ȼ�����Һ�п��Է�����Ӧ�����Ȼ��������Ȼ�ͭ��
��̽��˼·��:�������ʵ����ʲ�ͬ���ʵ��������,�ȷֱ�̽�������Ƿ���Fe(OH)3, Cu��,����С��Χ,Ȼ����ѡ���ʵ����Լ��ͷ���ͨ��ʵ��̽������ɡ� (װ���ڿ����е�ˮ������������̼���Բ���)
��ʵ��̽����:
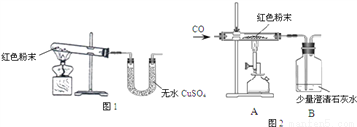
��1����ͬѧȡ������ɫ��ĩװ���Թ���,��ͼ1����ʵ�顣�����ˮ����ͭû�б���,�Ӷ��ų������е�_________��(������е����)
��2���ڼ�ͬѧʵ����۵Ļ�����,��ͬѧ��ȡ������ɫ��ĩ���Թ���,�μ�����ϡ����,��۲�,���ֹ���ȫ���ܽ�,��Һ��ɫ����ͬѧ��Ϊ�����ų������еĢٺ͢�,����ͬѧ��Ϊֻ���ų������,����Ϊ_________�Ĺ۵���ȷ(��"��"��"��")��
��3����ͬѧΪ��һ��ȷ����ɫ��ĩ�����,��ȡ5.0g�÷�ĩװ��Ӳ�ʲ�������,��ͼ2��ͨ����н���ʵ��.��ʼʱ����ͨ��CO����,��һ��ʱ����ټ���ʹ���ַ�Ӧ������Ӧ��ȫ��,ֹͣ����,�Լ���ͨCO����ֱ����������ȴ����Ӧǰ��������װ�ú����ʵ�������,���������±�:
��� | ��Ӧǰ | ��Ӧ�� |
���� | �����ܺͺ�ɫ��ĩ������Ϊ37.3g | �����ܺ�������������Ϊ36.1g |
���� | ϴ��ƿ����ʢ��Һ������Ϊ180.0g | ϴ��ƿ������������Ϊ183.1g |
���������ۡ�:
��1����װ������ͨCO�����������________��
��2��Ӧ��ѡ��_________���ʵ�����ݼ�����ȷ����ɫ��ĩ����ɡ����ռ���������:�ú�ɫ��ĩ������Dz����еĵ�_________��(�����)��
��3��ʵ���й۲쵽Aװ���е�����Ϊ___________��
��4��Ϊ�˷�ֹ��Һ����,��ʵ��ֹͣ����ǰ�Ƿ���Ҫ�ȶϿ�A��B�����Ӵ�?_______(��"��Ҫ"��"����Ҫ"),������________��
����˼���ۡ����ӻ����Ƕȣ�ͼ��ȱ��β������װ�á�
346 �� �ž�װ���п�������ֹ��ը�� �� 5 ���ֺ�ɫ��ĩ��� ����Ҫ ʵ�������һֱ��ͨһ����̼ ��������������Ҫ��������ʵ��ԭ����ʵ�����������衢װ�����Ӽ�ʵ����������۵ȷ�����п��顣�������ո�ʵ��ķ�Ӧԭ���Լ�ʵ��ע�������ǽ����������Ĺؼ��� ʵ��̽���� ��1�������ṩ�����ϣ������������ȷֽ�Ϊ��������ˮ����ɫ��ˮ����ͭ��ˮ���������Ⱥ�ɫ��ĩ�������ˮCuSO4...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������2018����꼶��һ��ģ�⿼�Ի�ѧ�Ծ� ���ͣ���ѡ��
���ӵ�ʳ�Ρ���ָ��ʳ���м��������ĵ����(KIO3)�����е�Ԫ�صĻ��ϼ�Ϊ
A. +l�� B. +3�� C. +5�� D. +7��
C ����������Ԫ����+1�ۣ���Ԫ����-2�ۣ��裺��Ԫ�صĻ��ϼ���x�������ڻ��������������ϼ۴�����Ϊ�㣬�ɵã���+1��+x+��-2����3=0����x=+5����ѡC���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���Ĵ�ʡ2018����꼶��ѧ�ڶ���Ի�ѧ�Ծ� ���ͣ���ѡ��
����Ϊ����ʵ�鷽���У������е���( )
A. ������ͨ�����ȵ�ͭ˿�����Գ�ȥ�����е�����
B. Ҫ����ˮ���Ƿ�����������ӣ��ɼ���BaCl2��Һ���۲��Ƿ������ɫ����
C. Ҫ��ȥCaCl2��Һ�е����ᣬ�ɼ��������̼��Ƴ�ַ�Ӧ�����
D. ��PH��ֽ��ʪ���ò�����պȡʳ�ð״�����ֽ�ϣ��ⶨ��PH���ⶨֵ��ƫ��
B ��������A���������ͭ��Ӧ��������ͭ����������������̼�Ȳ����ͭ��Ӧ���ܹ���ȥ���ʣ�����B����ˮ�пɼ���BaCl2��Һ����ʹ�����˰�ɫ����������ȷ���ó���Ϊ���ᱵ�����п�����̼�ᱵ���Ȼ��������Ҳ����˵��ˮ�к�����������ӣ������У���ȷ��C�����������CaCl2��Һ�м��������̼��ƣ�̼��Ʋ�����ˮ��ȴ�������ᷴӦ�����Ȼ��ƣ�����ȥ�������ֲ������µ����ʣ�����D����pH��ֽ�ⶨδ...�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com