


科目:初中化学 来源: 题型:阅读理解
| 序号 | 主要操作步骤 | 主要实验现象 | 化学反应方程式 | |
| ① | 在集气瓶中加入少量 |
|||
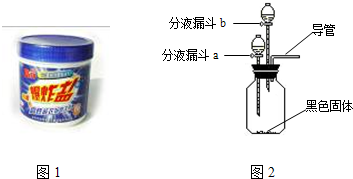
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 然后 |
||||
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢 | ||||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 将生成的气体通入 |
验证生成气体的成分. | |||
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠 | ||||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| A | B | C | D | |
| 分类标准 | 金属氧化物 | 非金属单质 非金属单质 |
盐 | 酸 酸 |
| 不属于该类别的物质 | CO2 CO2 |
Cu | Fe(OH)3 Fe(OH)3 |
H2O |
| 光照、叶绿素 |

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com