
分析 (1)根据降低水的硬度的方法分析;
(2)根据H2O和H2O2的分子结构不同分析;
(2)根据Na2CO3和CaCO3在水中的溶解性不同分析;
(4)根据pH的测定方法来分析;
解答 解:(1)生活中常用煮沸的方法降低水的硬度;
(2)水(H2O)和过氧化氢(H2O2)的组成相同但分子结构不同,所以化学性质一定不同;
(3)实验室中可通过Na2CO3和CaCO3在水中溶解性的不同加以区别,碳酸钠的溶解性对碳酸钙好的多.
(2)通常用pH试纸来测定溶液的酸碱度;
故答案为:(1)煮沸;(2)分子结构;(3)溶解性;(4)pH试纸;
点评 本题考查硬水软化的方法,物质的微观构成,物质的溶解性比较,测定溶液酸碱度的方法等,难度不大,要熟练掌握.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:选择题
| A. | 化学变化都遵循质量守恒定律,所以质量不发生改变的变化就是化学变化 | |
| B. | 化合物是由多种元素组成的纯净物,所以由多种元素组成的纯净物一定是化合物 | |
| C. | 最外层达8电子的微粒化学性质稳定,因此化学性质稳定的微粒最外层电子数都是8 | |
| D. | 燃烧是发光、放热的变化,所以有发光、放热现象的变化一定是燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 钢铁的冶炼是人类文明的一个重要标志,如图是模拟炼铁的实验装置图.
钢铁的冶炼是人类文明的一个重要标志,如图是模拟炼铁的实验装置图.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HNO3 Ca(OH)2 NaCl | B. | KNO3 CuCl2 Na2SO4 | ||
| C. | NaOH MgSO4 BaCl2 | D. | HCl Na2CO3 Ca(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
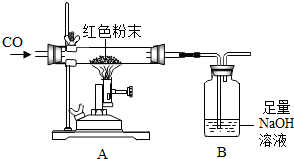 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为48.3g | 玻璃管和固体物质的总质量为47.1g |
| Ⅱ 组 | 洗气瓶和瓶中所盛物质的总质量为258.6g | 洗气瓶和瓶中所盛物质的总质量为261.91g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com