
现将100 g溶质质量分数为9.8%的稀硫酸与一定质量的氯化钡溶液恰好完全反应后,过滤得到284.7 g滤液。计算:
(1)生成硫酸钡沉淀的质量。
(2)氯化钡溶液中溶质的质量分数。
科目:初中化学 来源:甘肃省武威市、武威爱华育新学校,新起点学校,武威十三中2019-2010学年九年级下学期开学考试化学试卷 题型:计算题
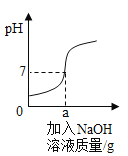
用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如图所示。请计算
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水_____克。
(2)当a为80g时,所得溶液中溶质的质量分数是多少____________(结果精确到0.1%)?
查看答案和解析>>
科目:初中化学 来源:2020年安徽省中考模拟化学试卷 题型:单选题
逻辑推理是学习化学常用的思维方法,下列根据实验现象推出的实验结论正确的是()
A.某气体不能使带火星的木条复燃,该气体一定不含氧气
B.金属铝能与硫酸铜溶液反应,铝的活动性强于铜的活动性
C.纸张燃烧后,余烬的质量比原纸张的质量小,该反应不遵循质量守恒定律
D.碳酸钠溶液和氢氧化钙反应后,向溶液中滴加无色酚酞溶液,溶液变红,说明氢氧化钙有剩余
查看答案和解析>>
科目:初中化学 来源:中考题原创:2011年度背景资源“中考题原创”(八则) 题型:填空题
我国各地食盐碘含量可以根据当地人群实际碘营养水平,在规定范围内浮动添加。下表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明,则回答下列问题:
产品标准号 | 一级品,净含量500g |
配料表 | 精制盐、碘酸钾、抗结剂 |
含碘量 | 20-30mg/kg |
储藏方式 | 密封避光、防潮 |
食用方法 | 烹调时待食品熟后加入碘盐 |
(1)“加碘盐”是在食盐中加入一定量的碘酸钾,则碘盐属于______物,食用碘盐可以有效地预防碘盐缺乏病,智力元素碘是人体内合成_____的主要原料之一。若人在幼年时期甲状腺激素分泌不足,可能会患_______。
(2)从上述说明中的食用方法和贮藏指南,可推测碘酸钾的化学性质之一为_______。
(3)盐业公司制造碘盐时并不直接使用碘单质,而是使用碘酸钾,主要原因可能是(____)
A碘酸钾的价格较低,有利于减轻居民食用碘盐的经济负担
B碘酸钾较易溶解于水,有利于碘盐生产操作和食用吸收
C碘酸钾热稳定性优于碘,有利于碘盐生产、贮放、使用过程中减少碘的损失
(4)碘是一把双刃剑,人体内的碘过量也会引起甲状腺疾病。青少年每天碘元素适宜摄入量约为0.15mg,假设这些碘元素主要是从碘盐中摄取,若1000g碘盐中含碘20mg,则你每天需食用碘盐____g。
(5)辨别真假碘盐的正确方法是________,将少量食盐撒到切开的土豆切面上,如果马上发现新鲜的土豆变成蓝色,那就是货真价实的加碘食盐,因为碘盐挥发出少量的碘单质,土豆中淀粉遇碘单质会变成___色。
查看答案和解析>>
科目:初中化学 来源:中考题原创:2011年度背景资源“中考题原创”(八则) 题型:填空题
2011年11月28日至12月9日,南非德班国际气候大会召开,以CO2为主的温室气体排放再次成为各国关注的焦点。则回答:
(1)《京都议定书》第一承诺期将于2012年到期,其核心内涵是减少温室气体的排放量,以控制全球的气候变暖。下列导致温室效应的主要气体是(____)
a.二氧化碳 b.氧气 c.氮气 d.氢气
(2)“碳汇”是指从空气中清除和吸收二氧化碳的过程与机制。为了应对气候变化,减少全球温室气体排放,其重要原则有:
①拒用原则。请举出低碳生活的一个实例:_____________。
②再生原则。开发和利用清洁而高效的新能源替代传统能源,如图是科学家设计的一种理想的氢元素循环模式,它实现了低碳减排,请写出(Ⅰ)中发生反应的化学方程式为______________________。
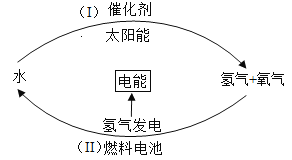
③回收原则。目前使用膜分离法从空气中分离出CO2 ,这个过程CO2发生_______(填“物理”或“化学”)变化。这些CO2可作为气体肥料,还可制造用于__________。
查看答案和解析>>
科目:初中化学 来源:2020年河北省沧州市中考模拟化学试卷 题型:简答题
化学与我们生产生活息息相关,请用所学知识填空.
(1)各种洗涤剂广泛进入人们的生活中,下列洗涤过程中所用洗涤剂具有乳化功能的是____________.
A.用沐浴露洗澡 B.用洗洁精清洗餐具上的油污 C.用汽油除去衣服上的油污 D.用肥皂液洗衣服
(2)随着塑料制品进入千家万户,生活中废弃的塑料垃圾越来越多,形成难于处理的环境污染物,造成所谓“__”.
(3)催化剂在生产生活中有重要作用,如在汽车上安装尾气催化转化器,将尾气中有毒的CO和NO在催化剂作用下转化为能够参与大气循环的CO2和N2.请写出该过程的化学方程式____________________.
查看答案和解析>>
科目:初中化学 来源:2020年广东省九年级一模化学试卷 题型:计算题
某食用碱的主要成分是 Na2CO3,其中含有少量的 NaCl,小明同学为测定该食用碱中 Na2CO3 的质量分数,他进行了以下实验,取 40 g 食用碱,加水配成 400g 的溶液,把溶液平均分为四份,然后分别加入一定质量分数的 CaCl2 溶液,实验数据见下表:
实验一 | 实验二 | 实验三 | 实验四 | |
食用碱的质量/g | 10 | 10 | 10 | 10 |
加入CaC12溶液的质量/g | 20 | 40 | 60 | 80 |
生成沉淀的质量/g | 2.5 | 5 | m | 8 |
请分析表中数据并计算回答。
(1)m=________;
(2)40 g 该食用碱配成的溶液与足量 CaCl2 溶液反应,最多生成沉淀质量为_____g;
(3)该食用碱中 Na2CO3 的质量分数是多少_____?(写出计算过程,答案精确到 0.1%)
(4)请根据实验四的数据画图并标上合适的坐标数据_____。
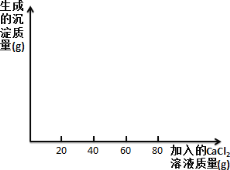
查看答案和解析>>
科目:初中化学 来源:河北省唐山市遵化市2019-2020学年九年级下学期期中化学试卷 题型:单选题
钠是人体必需的常量元素,下图是钠原子结构示意图。下列说法正确的是
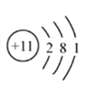
A. 钠的相对原子质量为11g B. 钠原子在化学反应中易失去电子
C. 钠由液态变成气态,微粒间间隔变小 D. 人体缺钠会导致甲状腺疾病
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com