
分析 (1)根据石灰水高温煅烧后生成物的性质解答;
(2)根据二氧化碳的质量,可求参加反应的碳酸钙的质量,从而可求石灰石中碳酸钙的质量分数.
(3)根据求碳酸钙质量分数所需数据来解答;
(4)方案Ⅲ是根据生成碳酸钙质量来计算石灰石中碳酸钙的质量分数,其中生成二氧化碳质量是关键.
解答 解:(1)石灰石高温煅烧后生成氧化钙和二氧化碳,氧化钙能吸收空气中的水分,冷却时要在密闭干燥容器中进行;
(2)因为剩余固体质量6.04g包含了杂质质量,所以得出碳酸钙的质量分数超过100%;
生成二氧化碳质量=10g-6.04g=3.96g,
设生成3.96g二氧化碳,需碳酸钙质量为x
CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 3.96g
$\frac{100}{x}=\frac{44}{3.96g}$
x=9g
CaCO3%=$\frac{9g}{10g}$×100%=90%
(3)方案Ⅱ是:碳酸钙与过量稀盐酸反应生成氯化钙,氯化钙和过量碳酸钠反应生成碳酸钙沉淀,生成碳酸钙的质量等于石灰石中碳酸钙的质量,其中只需知道稀盐酸与碳酸钠过量即可,不需知道具体数据,故选AC;
(4)方案Ⅲ是:根据生成的二氧化碳与氢氧化钙反应,生成碳酸钙质量来计算石灰石中碳酸钙的质量分数,而二氧化碳溶于水且导管中仍有部分二氧化碳未导出,计算得出的碳酸钙质量分数要比方案工和方案Ⅱ低,故选AB;
故答案为:
(1)剩余固体中的氧化钙能吸收空气中的水分;
(2)剩余固体质量6.04g包括了杂质的质量;90%;
(3)AC;
(4)AB.
点评 本题是运用化学中的基本思想质量守恒思想,通过归纳碳酸钙在不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.


科目:初中化学 来源: 题型:选择题
| A. | 2Mg+O2↑$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | H2O2+MnO2═H2O+MnO2+O2 | ||
| C. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | D. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
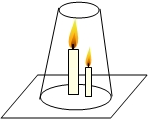 对“高低不同的燃着的蜡烛罩上茶杯后哪个先熄灭?”这一问题,甲、乙两名同学有不同的认识.甲同学认为高的蜡烛先熄灭,乙同学认为低的蜡烛先熄灭.谁也说服不了谁,于是他们设计了如图的实验来验证自己的猜想.(空气的密度是1.293g/L,二氧化碳的密度是1.977g/L)
对“高低不同的燃着的蜡烛罩上茶杯后哪个先熄灭?”这一问题,甲、乙两名同学有不同的认识.甲同学认为高的蜡烛先熄灭,乙同学认为低的蜡烛先熄灭.谁也说服不了谁,于是他们设计了如图的实验来验证自己的猜想.(空气的密度是1.293g/L,二氧化碳的密度是1.977g/L)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 紫色石蕊试液 | B. | 无色酚酞试液 | C. | pH试纸 | D. | 蓝色石蕊试液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com