
| A. | 苯中的C、H元素的质量比为12:1 | |
| B. | 苯是由6个碳元素和6个氢元素组成 | |
| C. | 苯分子中碳的原子结构示意图为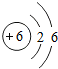 | |
| D. | 苯中碳、氢元素均位于元素周期表的第二周期 |
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
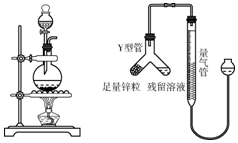
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水龙头坏了不停地流水,有时间再修理 | |
| B. | 农业浇灌推广使用喷灌、滴灌等技术代替大水漫灌 | |
| C. | 为保障工业用水,大力寻找水源并开凿水井 | |
| D. | 直接将生活污水排入江河中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
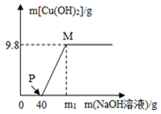 含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,则下列说法不正确的是( )
含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,则下列说法不正确的是( )| A. | m1的数值为80 | |
| B. | P点溶液中的溶质是氯化钠和氯化铜 | |
| C. | M点溶液中的溶质是氯化钠 | |
| D. | 整个反应过程中,溶液中氯离子个数不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
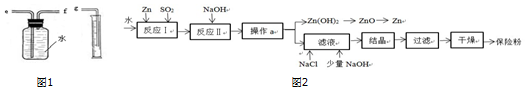
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 气球在上升时,不受重力的作用 | |
| B. | 气球升空到一定高度后,会发生爆炸 | |
| C. | 制作气球的材料可能是合成材料 | |
| D. | 向气球中充气时,气球中气体的分子间隔变小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com