
【题目】在实验室里称量一定质量的Na2CO3放入烧杯中,加入一定质量分数的稀硫酸100 g,恰好完全反应,共生成2.2 g的CO2气体(假设产生的气体完全逸出,水的挥发忽略不计)。已知实验中发生的化学反应:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
(1)Na2CO3样品的质量为_________________g。
(2)100 g稀硫酸的溶质质量分数为_______________(写出计算过程)。
(3)反应后烧杯中溶液的溶质质量分数为______________(写出计算过程,结果精确到0.1%)。
科目:初中化学 来源: 题型:
【题目】实验室现有下列仪器及部分药品(药品自选),请回答下列问题:
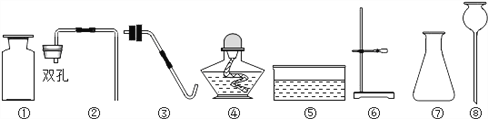
(1)仪器⑧的名称为_______________。
(2)利用上述仪器可以制取二氧化碳,你选择的仪器是________(填序号),反应的化学方程式为_____。
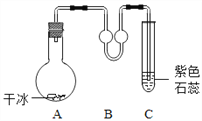
(3)常温下进行如下图所示实验。A 中固体逐渐减 少,发生__________(选填“物理”或“化学”)变 化。C 中有气泡,溶液颜色____。
(4)有同学称取了一定质量的铜锌合金样品,加入 到盛有 146.0g 稀盐酸的烧杯中,发现两者恰好完全反应(杂质不参加反应),且反应后烧杯内物质总质 量减少了 0.3g,请问该稀盐酸中溶质的质量分数为多少?__________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】微粒观是化学学科基本观念,下图中A、B、C、D是四种粒子的结构示意图。

请回答下列问题:
⑴ 图中A、B、C、D属于_______种元素的粒子;
⑵ A、B、C、D四种粒子中,不具备稳定结构的是_________(填序号);
⑶ D中x=________;
⑷ A与C形成化合物的化学式是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示,在白色点滴板1-6的孔穴中,分别滴加2滴紫色石蕊溶液。
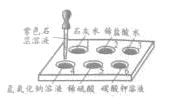
(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显 (填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有 (填孔穴序号,下同)。
(3)作为空白对照实验的孔穴是 。
(4)再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港海水资源丰富。
(l)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中除去粗盐中不溶性杂质获得精盐的步骤是:溶解→过滤→蒸发→计算产率等。
① 过滤操作中玻璃棒的末端要轻轻的斜靠在______一边。蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是______。
② 下列操作可能导致精盐产率偏高的是______(填字母)。
a.食盐没有完全溶解即过滤
b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。下图是从海水中获得氯化镁溶液的流程。
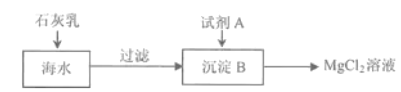
① 在海水中加人石灰乳后,发生反应的化学方程式是______________。
② 上述过程中试剂A与沉淀B 发生的是中和反应,则试剂A是(填名称)______。
(3)2017年5月18日,在中国南海海域实现可燃冰(CH4·nH2O)试采成功,这将使人类能源格局翻开新篇章。

① 可燃冰中,水分子形成一种空间笼状结构,甲烷和少虽N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于_________(选填“纯净物”或“混合物”)。
② 若某种可燃冰中CH4与H2O的质量比是1:9,则该可嫩冰中n=_______。
③ 可燃冰中甲烷完全燃烧的化学方程式是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室里称量一定质量的Na2CO3放入烧杯中,加入一定质量分数的稀硫酸100 g,恰好完全反应,共生成2.2 g的CO2气体(假设产生的气体完全逸出,水的挥发忽略不计)。已知实验中发生的化学反应:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
(1)Na2CO3样品的质量为_________________g。
(2)100 g稀硫酸的溶质质量分数为_______________(写出计算过程)。
(3)反应后烧杯中溶液的溶质质量分数为______________(写出计算过程,结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用铝土矿(只考虑含Al2O3及Fe2O3)生产Al的工艺流程如下,请回答下列问题:
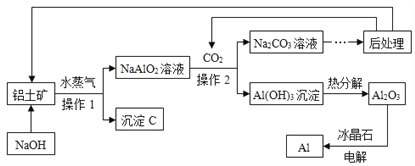
【查阅资料】:Ⅰ、铝土矿中Al2O3可以和NaOH溶液反应,反应的化学方程式为:Al2O3 + 2NaOH == 2NaAlO2 + 2H2O;Ⅱ、Fe2O3不和NaOH溶液反应。
(1)工业生产中,要将铝土矿细磨预处理,目的是_________;
(2)沉淀C的化学式是_________;
(3)操作1、操作2的名称是_________,实验室完成此操作时,需要的玻璃仪器的是玻璃棒、烧杯和_________;
(4)此工艺中,可循环使用的物质是CO2、H2O和_________;(填化学式)
(5)电解Al2O3的化学方程式为_________;
(6)NaAlO2溶液中通入CO2反应的化学方程式是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学欲配制一定溶质质量分数的NaCl溶液,他准备了下列实验仪器。
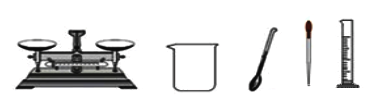
请填空:
(1)配制时可按下列实验步骤进行:
计算→称量→量取→_________。
(2)称量时,NaCl固体粉末应放在托盘天平______(填“左盘”或“右盘”)的纸片上。
(3)配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是__________(填仪器名称)。
(4)量取一定体积的水,除了用量筒外,还需要用_________(填仪器名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学用下图装置进行CO与Fe2O3的反应。下列说法错误的是

A.该实验装置应增加尾气处理装置
B.加热前应先通入一段时间的CO以排尽装置内的空气
C.NaOH溶液应改为Ca(OH)2溶液以检验产生的CO2气体
D.反应后的固体是Fe和Fe2O3的混合物,可以采用加入盐酸并过滤的方法得到Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com