
 某化学课外兴趣小组,开展了以下两项活动:
某化学课外兴趣小组,开展了以下两项活动: 实验过程中溶液的pH变化曲线如右图所示:
实验过程中溶液的pH变化曲线如右图所示:

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量白色固体放入足量水中 | 白色固体完全溶解 | |
| ②取①中少量溶液,加入 |
产生大量气泡 | 假设1成立 |
| ③另取①中少量溶液, |
假设2成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
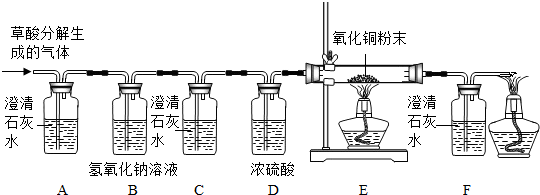
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| 380℃~400℃ |
| ||
| 380℃~400℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有 |
CO、CO2都有 |
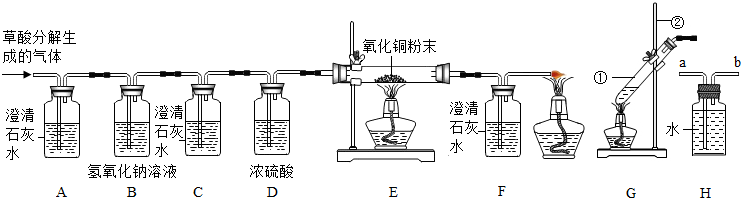
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com