
| A. | 黄酮素是由黄酮素分子构成的 | |
| B. | 氧元素的质量分数为9.0% | |
| C. | 黄酮素是由15个碳原子、10个氢原子和2个氧原子构成的 | |
| D. | 黄酮素中碳、氢、氧元素的质量比为15:10:2 |
分析 A.根据物质的构成来分析;
B.根据化合物中元素的质量分数来分析;
C.根据物质的构成来分析;
D.根据化合物中元素的质量比来分析.
解答 解:A.黄酮素是由黄酮素分子构成的,故正确;
B.黄酮素(C15H10O2)中氧元素的质量分数为$\frac{16×2}{12×15+1×10+16×2}×100%$≈14.4%,故错误;
C.黄酮素(C15H10O2)是由分子构成的,而不是由原子直接构成的,故错误;
D.黄酮素中碳、氢、氧元素的质量比为(12×15):(1×10):(16×2)=90:5:16,故错误.
故选A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:2017届广东省汕头市龙湖区九年级5月模拟考试化学试卷(解析版) 题型:探究题
如图1所示是实验室制取气体的装置,请回答:
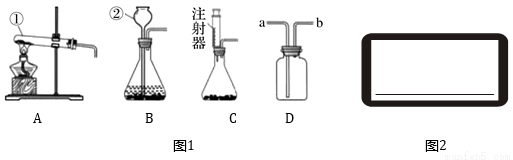
(1)写出有标号仪器的名称:①_________;②_________;
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为________________。若用D装置来收集氧气,气体应从_______(填“a”或“b”)端进入;
(3)在实验室里,二氧化碳常用石灰石与稀盐酸反应来制取.若要控制反应速率和节约药品,应选用的发生装置为_______(填序号);
(4)①用质量分数为37%的浓盐酸配制100g 10%的盐酸,除了用到胶头滴管、玻璃棒和和量筒外,还需补充的一种仪器是___________;
②将上述配制好的溶液装入试剂瓶中,盖好瓶塞并贴上标签。请在如图2所示的标签内填入相应的内容。_________
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 ”为铜片).
”为铜片).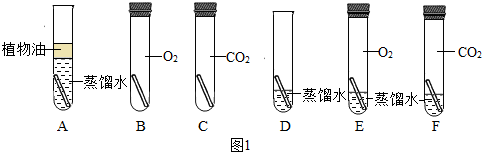
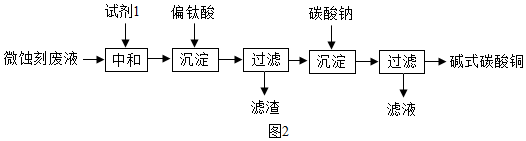
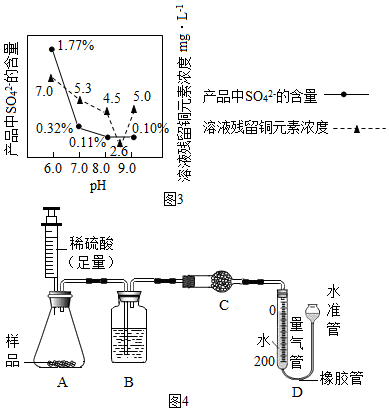
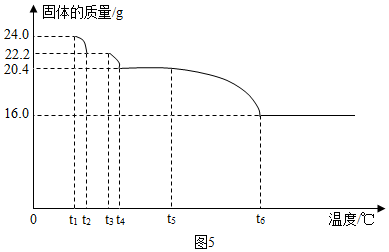
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝被广泛的应用于生产生活中,是因为铝的化学性质稳定 | |
| B. | 使用煤炉要防止中暑,是因为煤不充分燃烧产生的一氧化碳有毒 | |
| C. | 近视镜矫正近视是利用凹透镜对光有会聚作用 | |
| D. | 运动鞋鞋底有花纹是因为增大受力面积从而增大摩擦力 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 当水沸腾时,烧杯内气泡上升过程中受到水的压强变大 | |
| B. | 烧杯口有大量的“白气”冒出,这些“白气”是水蒸气遇冷后液化成的小水滴 | |
| C. | 水的沸点为98℃,此时烧杯内水面上方的气压小于1标准大气压 | |
| D. | 水在加热过程中,吸收热量,温度升高;沸腾时,吸收热量,温度不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
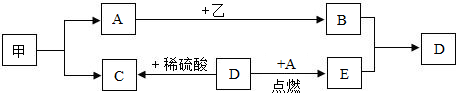
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com