
| 实验装置 | 实验现象 | 实验结论 |
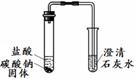 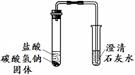 实验Ⅰ 实验Ⅱ | 实验I、II中均观察到:白色固体逐渐减少, ;澄清石灰水变浑浊。 | Na2CO3和NaHCO3都能与盐酸反应产生CO2;NaHCO3与盐酸反应的化学方程式是 。 |
| | t1/℃ | t2/℃ | t3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:初中化学 来源:不详 题型:推断题
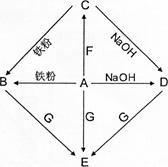
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 序号 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 氯化钾与氯化铵固体 | 熟石灰、研磨 |
| B | 硝酸铵与食盐固体 | 水 |
| C | 氢氧化钠溶液与碳酸钠溶液 | 酚酞溶液 |
| D | 一氧化碳与二氧化碳气体 | 澄清的石灰水 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
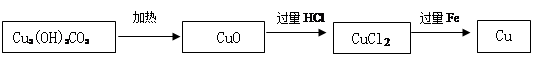
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题
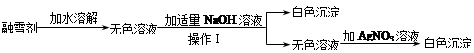
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题
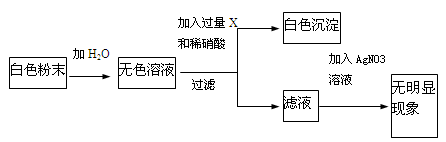
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 选项 | 物质 | 少量杂质 | 所加试剂或方法 |
| A | CaCl2溶液 | HCl | 过量的CaC03 |
| B | H2 | 水蒸气 | 通过浓硫酸洗气 |
| C | H20 | 异味 | 加入明矾 |
| D | NaCl | Na2C03 | 加水溶解,加Ca(N03)2溶液、过滤、蒸发、结晶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com