
| A. | Cu | B. | Zn | C. | Mg | D. | Al |
分析 依据金属反应时生成的氢气质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,可以判断等质量的锌、镁、铝三者反应时生成的氢气关系,而后利用极端假设法判断5.6g金属全部是铁时的氢气量,据此判断混入的金属即可;
解答 解:由于该铁片全部溶解,说明成分都与稀盐酸反应,故不可能为铜;
假设5.6g全是铁时生成的氢气量是x
Fe+H2SO4=FeSO4+H2↑
56 2
5.6g x
$\frac{56}{5.6g}=\frac{2}{x}$
x=0.2g
因此混入的金属等质量时生成的氢气要比铁少,由于氢气质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,所以锌、镁、铝三种金属中等质量的锌比铁生成的氢气要少;
故选B.
点评 若能熟练掌握等质量的镁、铝、锌、铁四种金属完全反应放出氢气由多到少的顺序为铝、镁、铁、锌,会对解决此类问题有很大帮助.


科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳和氮气 | B. | 二氧化碳和二氧化氮 | ||
| C. | 二氧化碳和氧气 | D. | 二氧化碳、氮气和氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
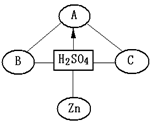 构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,A、B、C属于不同类别的化合物,且它们发生的反应均属于复分解反应.
构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,A、B、C属于不同类别的化合物,且它们发生的反应均属于复分解反应.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
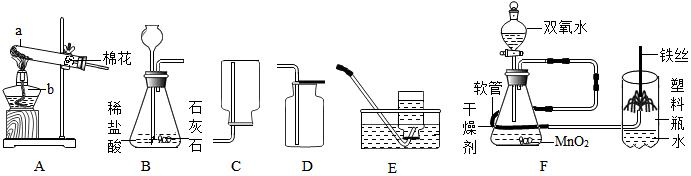
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生锈的铁钉与盐酸反应后可得到氯化铁溶液 | |
| B. | 紫色石蕊试液遇到酸变红色 | |
| C. | 氢氧化铜可以溶解在稀硫酸中 | |
| D. | 任何酸都能与氯化钡溶液反应生成白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com