
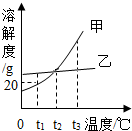
 根据如图的溶解度曲线,判断下列说法不正确的是( )
根据如图的溶解度曲线,判断下列说法不正确的是( )| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | t1℃时,甲的饱和溶液中溶质和溶剂的质量比为1:5 | |
| C. | t2℃时,甲、乙两物质的溶解度相等 | |
| D. | 将t3℃时甲、乙两物质的饱和溶液降温到t1℃,甲析出的晶体多 |
分析 根据溶解度曲线的意义进行分析解答,在同一温度下,对应的溶解度曲线越高,则溶解度越大;饱和溶液是指在一定温度下在一定量的溶剂里不能再溶解某种溶质的溶液,据此解答.
解答 解:A、具有可以看出,甲物质的溶解度随温度的升高而增大,正确;
B、t1℃时,甲的溶解度为20g,则甲的饱和溶液中溶质和溶剂的质量比为20g:100g=1:5,正确;
C、t2℃时,甲、乙两物质的溶解度相交于一点,表示在该温度下二者的溶解度相等,正确;
D、将t3℃时甲、乙两物质的饱和溶液降温到t1℃,因为不知道溶液质量的大小,故无法比较析出晶体的大小,错误;
故选D.
点评 明确溶解度定义及曲线的含义是解答本题关键,要掌握溶解度曲线的意义以便做出正确判断.


 名师指导一卷通系列答案
名师指导一卷通系列答案科目:初中化学 来源: 题型:解答题
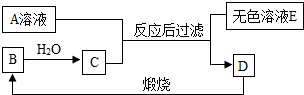 A、B、C、D是生活中常见的物质.已知A是含三种元素的钠盐,D是大理石的主要成分,它们之间的关系如图所示.请回答下列问题:
A、B、C、D是生活中常见的物质.已知A是含三种元素的钠盐,D是大理石的主要成分,它们之间的关系如图所示.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在“侯式联合制碱法”的工艺流程中,最后一步是用加热碳酸氢钠的方法来制取纯碱.某纯碱生产厂制得的样品Na2CO3中混有少量NaHCO3.为了测定样品中Na2CO3的质量分数,取100g混合物加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,Na2CO3受热不分解),反应过程中生成二氧化碳气体的质量与反应时间的关系如图所示.
在“侯式联合制碱法”的工艺流程中,最后一步是用加热碳酸氢钠的方法来制取纯碱.某纯碱生产厂制得的样品Na2CO3中混有少量NaHCO3.为了测定样品中Na2CO3的质量分数,取100g混合物加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,Na2CO3受热不分解),反应过程中生成二氧化碳气体的质量与反应时间的关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水的分解过程有能量的变化 | |
| B. | 氢气燃烧生成能使石灰水变浑浊的气体 | |
| C. | 水的合成过程中原子不发生变化 | |
| D. | 水的分解实验证明水是由氢氧两种元素组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
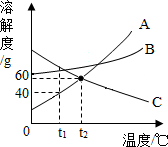 如图A、B、C三种固体物质的溶解度曲线.
如图A、B、C三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
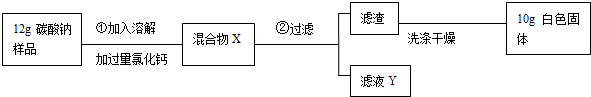
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 具有相同核电荷数(即核内质子数)的一类原子的总称 | |
| B. | 是相对原子质量相同的一类原子的总称 | |
| C. | 是具有相同电子数的一类原子的总称 | |
| D. | 是具有相同中子数的一类原子的总称 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 7.2g | B. | 5.8g | C. | 4.4g | D. | 9.5 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com