
分析 根据锌的质量结合方程式计算生成氢气的质量,生成的硫酸锌的质量,反应后溶液的质量=反应前各组份的质量之和-气体的质量,并依据溶质的质量分数计算较多.
解答 解:设生成氢气的质量为x,生成硫酸锌的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 161 2
13g y x
$\frac{65}{13g}$=$\frac{161}{y}$=$\frac{2}{x}$
x=0.4g
y=32.2g
反应后所得溶液中硫酸锌的质量分数为:$\frac{32.2g}{100g+13g-0.4g}$×100%=28.6%.
答:生成氢气的质量为0.4g.完全反应后所得溶液中溶质的质量分数28.6%.
点评 根据质量守恒定律,反应后所得溶液的质量=参加反应金属的质量+加入的稀硫酸的质量-放出气体的质量,并掌握方程式计算的解题格式,溶质的质量分数的计算方法.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
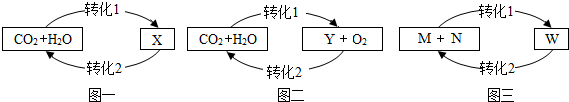
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
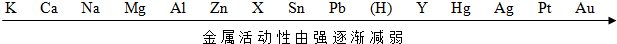
| A. | X可与Y(NO3)2溶液反应 | B. | X可与盐酸反应 | ||
| C. | Y可与AgNO3溶液反应 | D. | Y可与稀H2SO4反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | K2CO3 KCl Na2SO4 | B. | KNO3 Na2SO4 NaCl | ||
| C. | (NH4)2SO4 FeCl3 KOH | D. | CuSO4 BaCl2 NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 简要回答下列问题:
简要回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液:由溶剂和溶质组成 | |
| B. | 饱和溶液:不能继续溶解溶质的溶液 | |
| C. | 不饱和溶液:还能溶解溶质的溶液 | |
| D. | 溶解度:在一定量的溶剂中溶解溶质的最大值 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
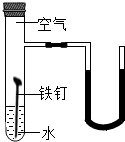 请回答下列有关金属的问题.
请回答下列有关金属的问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com