
 .
. 分析 (1)由分子构成的物质,分子是保持物质的化学性质的最小粒子.
(2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
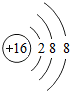
(3)质子数为16的硫离子,是原子得到2个电子得到的,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有8个电子,据此进行分析解答.
解答 解:(1)甲烷是由甲烷分子构成的,保持甲烷的化学性质的最小粒子是甲烷分子,其分子符号为CH4.
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.铵根离子可表示为NH4+.
(3)质子数为16的硫离子,是原子得到2个电子得到的,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有8个电子,其离子结构示意图为: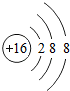 .
.
故答案为:(1)CH4;(2)NH4+;(3) .
.
点评 本题难度不大,掌握常见化学用语(分子符号、离子结构示意图、离子符号等)的书写方法是正确解答此类题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | Fe(Cu) | 加过量FeSO4溶液、过滤 |
| B | CaO(CaCO3) | 加足量的水、过滤 |
| C | NaCl溶液(Na2CO3) | 加入适量的CaCl2溶液、过滤 |
| D | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 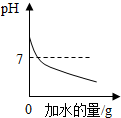 向pH=11的NaOH溶液中不断加水 | B. | 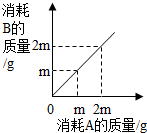 可表示硫与氧气反应时的质量关系 | ||
| C. | 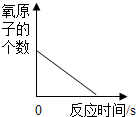 在密闭容器中红磷燃烧 | D. | 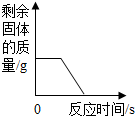 木炭还原氧化铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
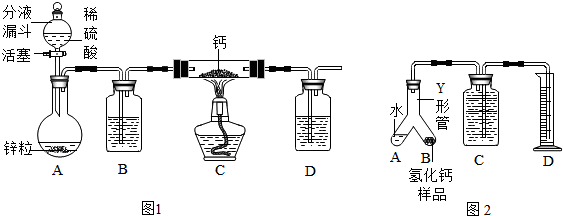
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com