
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据稀盐酸是氯化氢的水溶液,以及参加反应的碳酸钙质量进行分析;
(3)根据稀盐酸和碳酸钙反应生成氯化钙,依据题中的数据进行计算.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)设参加反应的盐酸质量为x,生成氯化钙质量为y,二氧化碳质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 18 44
12.5g×20% x y z
$\frac{100}{12.5g×20%}$=$\frac{73}{x}$=$\frac{111}{y}$=$\frac{44}{z}$
x=1.825g
y=2.775g
z=1.1g
所以反应后溶液的质量为:12.5g×20%+34.4g-1.1g=35.8g.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)HCl,1.825;
(3)氯化钙溶液,CaCl2,2.775,35.8.
点评 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水能无限溶解任何物质且溶解时都不会吸热或放热 | |
| B. | 生命活动离不开水 | |
| C. | 净化水的方法有吸附、沉淀、过滤和蒸馏等 | |
| D. | 用肥皂水可以检验硬水和软水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 制取气体时,先装药品,后检查装置的气密性 | |
| B. | 加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管 | |
| C. | 加热试管内的药品时,先预热,再加热 | |
| D. | 点燃可燃性气体时,先点燃使用,后验纯 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生成了2.2g CO2 | B. | 剩余CaCO3的质量为10.0g | ||
| C. | 生成了10.6g CaO | D. | 原来CaCO3的质量为15.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学用语是九年级化学的重要学习内容之一,也是学好化学的关键之一.请根据要求填写相应的化学符号.
化学用语是九年级化学的重要学习内容之一,也是学好化学的关键之一.请根据要求填写相应的化学符号.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加AgNO3溶液 |
| 实验操作 | 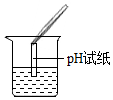 | 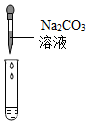 |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com