解:(1)钢铁是铁的合金,主要成分是铁,含有碳、硅等杂质,属于混合物.
(2)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.
(3)为了防止钢铁的锈蚀,人们常采用在其表面刷油漆或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水
(4)铁锈的主要成分氧化铁与盐酸反应生成氯化铁和水,化学方程式为
(5)铁可用来制作铁锅、车皮等;配制波尔多液的原料中含有硫酸铜溶液,铁能和硫酸铜溶液反应,化学方程式为
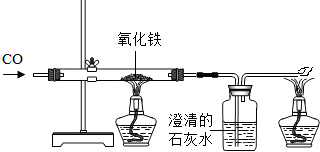
(6)二氧化碳和碳在高温条件下反应能生成一氧化碳,反应的化学方程式为:CO
2+C

2CO;
CO具有还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe
2O
3+3CO

2Fe+3CO
2.
(7)50%以上的废钢铁得到了回收利用,其目的是节约金属资源.
(8)氧化铁中铁元素的质量即为生成的铁的质量,即1000t×80%×
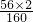
=560t
故答案为:(1)混合物 (2)水蒸气 氧气(无前后顺序) 酸碱性 (3)隔绝氧气
(4)Fe
2O
3+6HCl=2FeCl
3+3H
2O
(5)Fe+CuSO
4=FeSO
4+Cu
(6)排除硬质玻璃管中的空气,防止加热时爆炸
C+CO
2 
2CO Fe
2O
3+3CO

2Fe+3CO
2(7)节约金属资源
(8)560吨
分析:(1)根据钢铁组成成分进行分析判断.
(2)根据铁锈蚀的条件进行分析解答.
(3)铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈.
(4)根据氧化铁与盐酸反应的生成物写出化学方程式
(5)根据铁与硫酸铜溶液反应写方程式
(6)二氧化碳和碳在高温条件下反应能生成一氧化碳,一氧化碳和氧化铁在高温条件下反应能生成铁和二氧化碳,写出反应的化学方程式即可.
(7)根据废钢铁回收利用的意义进行分析判断.
(8)根据元素质量守恒,氧化铁中铁元素的质量即为生成的铁的质量.
点评:本题考查了与铁有关的知识,明确铁与铁合金,铁的生锈及防锈,铁的化学性质及用途是解答本题关键.


 2CO;
2CO; 2Fe+3CO2.
2Fe+3CO2.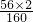 =560t
=560t 2CO Fe2O3+3CO
2CO Fe2O3+3CO  2Fe+3CO2
2Fe+3CO2


 钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.
钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.